Thiết kế protein

Thiết kế protein là một lĩnh vực thay đổi nhanh chóng với tiềm năng cách mạng hóa y học, công nghệ và môi trường. Nguồn: ipd.uw.edu.
Hai thập kỷ trước, David Baker (Đại học Washington, Mỹ) và các đồng nghiệp của ông đã đạt được thành tựu mang tính bước ngoặt khi sử dụng các công cụ tính toán để thiết kế một loại protein hoàn toàn mới. Ngày nay, khả năng thiết kế protein mới đã được phát triển để tạo ra các enzyme và protein theo yêu cầu. Phần lớn sự tiến bộ đó xuất phát từ các bộ dữ liệu ngày càng lớn về liên kết chuỗi trong protein và cấu trúc, kết hợp với các phương pháp nghiên cứu học sâu phức tạp.
Sử dụng chiến lược dựa trên trình tự gen, các mô hình ngôn ngữ lớn với sự hỗ trợ của AI giúp xử lý các chuỗi protein. Noelia Ferruz thuộc Viện Sinh học Phân tử Barcelona (Tây Ban Nha) đã phát triển một thuật toán có tên ProtGPT2, có thể liên tục tạo ra các protein tổng hợp có khả năng gấp nếp ổn định khi được sản xuất trong phòng thí nghiệm. Một công cụ khác do Ferruz và các đồng nghiệp phát triển, được gọi là ZymCTRL, dựa trên trình tự thành phần protein và dữ liệu chức năng để thiết kế các loại protein của các enzyme có trong tự nhiên, enzyme là chất xúc tác sinh học có thành phần cơ bản là protein. Protein được tạo thành từ hàng trăm hoặc hàng nghìn axit amin, chúng được gắn với nhau thành chuỗi dài. Trong quá khứ, các phương pháp tiếp cận dựa trên trình tự chuỗi có thể xây dựng và điều chỉnh các tính năng hiện có của protein để hình thành các khung cấu trúc protein mới, nhưng chúng kém hiệu quả hơn khi thiết kế riêng cho các thành phần cấu trúc protein hoặc các tính năng.
Năm 2023, chúng ta đã chứng kiến sự tiến bộ đáng chú ý trong thuật toán thiết kế protein. Một số mô hình phức tạp sử dụng mô hình khuếch tán. Các thuật toán này ban đầu được đào tạo để học cách phân biệt các yếu tố cấu trúc protein thực tế với các cấu trúc không thực tế, chúng có khả năng xây dựng các cấu trúc hợp lý về mặt sinh học, do người dùng xác định. Phòng thí nghiệm của Công ty Generate Biomedicines (Mỹ) đã xây dựng thành công phần mềm RF có khả năng thiết kế các protein mới với giao diện phù hợp theo yêu cầu. Phiên bản mới hơn của phần mềm RF cho phép các nhà thiết kế định hình một cách có tính toán các protein xung quanh các mục tiêu phi protein như DNA, các phân tử nhỏ và thậm chí cả các ion kim loại. Tiến bộ này sẽ mở ra những chân trời mới cho các enzyme được thiết kế, các bộ điều chỉnh phiên mã di truyền, các vật liệu sinh học chức năng...
Phát hiện deepfake
Sự bùng nổ của các thuật toán AI tạo sinh và sự thuận tiện trong tiếp cận đã giúp việc tổng hợp, xây dựng các hình ảnh, âm thanh và video hoàn toàn nhân tạo trở nên đơn giản và ngày càng “thật” hơn. Điều này có thể mang tới những trải nghiệm thú vị cho người dùng, xong cũng có nguy cơ tạo ra nhiều bất ổn chính trị. Siwei Lyu - một nhà khoa học máy tính tại Đại học Buffalo (Mỹ) cho biết, ông đã thấy rất nhiều hình ảnh và âm thanh deepfake do AI tạo ra liên quan đến cuộc xung đột Israel-Hamas, nhiều nội dung được tạo ra với mục đích lừa đảo.
Để chống lại điều này, các nhà khoa học như Siwei Lyu đang phát triển nhiều công cụ phát hiện deepfake. Các thuật toán mới có thể nhận ra sự khác biệt giữa nhân vật giả mạo và nhân vật thật. Ví dụ, các nếp gấp ở tai ngoài của một người cũng có thể tiết lộ sự không khớp giữa khuôn mặt và đầu, trong khi những điểm bất thường ở răng có thể tiết lộ các video bắt chước giọng nói đã qua chỉnh sửa, trong đó miệng của một người được điều khiển bằng kỹ thuật số để nói những điều mà đối tượng thật không nói... Chương trình pháp y ngữ nghĩa của Cơ quan Nghiên cứu các Dự án tiên tiến quốc phòng Mỹ đã phát triển một bộ công cụ hữu ích để phân tích deepfake. Hay gần đây, nhóm nghiên cứu của Lyu đã phát triển DeepFake-O-Meter (kho tập trung lưu trữ thuật toán công khai giúp phân tích video từ các góc độ khác nhau để phát hiện nội dung deepfake). Những công cụ như vậy sẽ hữu ích, nhưng có lẽ cuộc chiến chống lại thông tin sai lệch do AI tạo ra sẽ còn kéo dài trong nhiều năm tới.
Chèn những đoạn lớn DNA
Vào cuối năm 2023, các cơ quan quản lý của Mỹ và Vương quốc Anh đã phê duyệt liệu pháp chỉnh sửa gen dựa trên CRISPR lần đầu tiên đối với bệnh thiếu máu hồng cầu lưỡi liềm và bệnh Beta thalassemia phụ thuộc truyền máu (căn bệnh khiến bệnh nhân phải truyền máu định kỳ, nếu không sẽ có nhiều biến chứng và giảm tuổi thọ).
CRISPR và các dẫn xuất của nó sử dụng một đoạn RNA ngắn có thể được lập trình để điều hướng enzyme cắt DNA như Cas9 đến một vị trí gen cụ thể. Chúng thường được sử dụng trong phòng thí nghiệm để vô hiệu hóa các gen khiếm khuyết và tạo ra những thay đổi nhỏ về trình tự gen. Việc chèn chính xác và có thể lập trình các chuỗi DNA lớn hơn bao gồm hàng nghìn nucleotide là rất khó, nhưng các giải pháp mới có thể cho phép các nhà khoa học thay thế các đoạn quan trọng của gen khiếm khuyết hoặc chèn các chuỗi gen đầy đủ chức năng. Le Cong, một nhà di truyền học phân tử tại Đại học Stanford (Mỹ) và các đồng nghiệp đã khám phá các protein ủ sợi đơn (SSAP - Single Strand Annealing Protein), là các phân tử có nguồn gốc từ virus làm trung gian cho quá trình tái tổ hợp DNA. Khi kết hợp với hệ thống CRISPR-Cas (trong đó chức năng cắt DNA của Cas9 đã bị vô hiệu hóa), các SSAP này cho phép chèn mục tiêu chính xác lên đến 2 kilobase DNA vào bộ gen của con người.
Bên cạnh đó, còn có phương pháp khác khai thác cách thức dựa trên CRISPR là chỉnh sửa gốc để đưa ra các chuỗi ngắn nhằm sàng lọc có chọn lọc các enzym để có thể ghép chính xác các đoạn DNA lớn vào bộ gen. Phương pháp này gọi là PASTE (Programmable Addition through Site-Specific Targeting Elements), có nhiều tiềm năng cho việc chỉnh sửa ngoài cơ thể (ex vivo) các tế bào được nuôi cấy và có nguồn gốc từ bệnh nhân.
Những phương pháp chỉnh gen không chỉ phục vụ sức khỏe con người. Mới đây, nhóm nghiên cứu do Caixia Gao dẫn đầu tại Viện Khoa học Trung Quốc đã phát triển PrimeRoot - một phương pháp sử dụng chỉnh sửa gốc để nhắm đến các vị trí cụ thể mà enzyme có thể sử dụng để chèn tới 20 kilobase DNA vào cả lúa và ngô. Caixia Gao cho biết, kỹ thuật này giúp cây trồng tăng khả năng kháng bệnh. Đây chỉ là một ví dụ điển hình trong làn sóng đổi mới sáng tạo của kỹ thuật chỉnh sửa bộ gen thực vật dựa trên CRISPR.
Kết nối não với máy tính
Căn bệnh xơ cứng teo cơ một bên đã khiến Pat Bennett không thể diễn đạt bằng lời nói. Sau khi được điều trị, Bennett đã có sự phục hồi đáng chú ý khi nói được 62 từ mỗi phút với vốn từ vựng 125.000 từ (nhiều hơn gấp đôi vốn từ vựng của một người nói tiếng Anh trung bình). Tất cả là nhờ vào một thiết bị kết nối não với máy tính (BCI - Brain Computer Interface) phức tạp được phát triển bởi nhà thần kinh học Francis Willett thuộc Đại học Stanford và các đồng nghiệp của ông tại Tập đoàn BrainGate, Mỹ. Willett và các đồng nghiệp đã cấy các điện cực vào não của Bennett để theo dõi hoạt động của tế bào thần kinh, sau đó huấn luyện các thuật toán học sâu để chuyển những tín hiệu đó thành lời nói. Các nhà nghiên cứu cũng đang áp dụng những mô hình ngôn ngữ dựa trên AI để tăng tốc độ giải thích thông tin mà bệnh nhân đang cố gắng truyền đạt.
Leigh Hochberg, nhà thần kinh học tại Đại học Brown, đồng thời là giám đốc của tập đoàn BrainGate (Mỹ) cho biết, những tiến bộ này bắt nguồn từ sự tích lũy kiến thức liên tục về giải phẫu thần kinh chức năng trong não người. Với sự hỗ trợ của máy học, những kiến thức đó ngày càng được phân tích chi tiết để tìm ra cách đặt các điện cực tốt hơn và giải mã nhanh hơn các tín hiệu mà điện cực thu được. Bên cạnh tiềm năng điều trị các chứng suy giảm nhận thức, rối loạn tâm trạng, lĩnh vực này cũng đang chứng kiến sự tiến bộ trong việc hỗ trợ người bệnh di chuyển hoặc điều khiển các bộ phận trên cơ thể.
Độ phân giải siêu cao
Stefan Hell, Eric Betzig và William Moerner đã được trao giải Nobel Hóa học năm 2014 vì tìm ra phương pháp phá vỡ giới hạn nhiễu xạ làm hạn chế độ phân giải không gian của kính hiển vi quang học. Độ chi tiết thu được ở mức hàng chục nanomet đã mở ra một loạt thí nghiệm hình ảnh ở quy mô phân tử. Tuy nhiên, các nhà nghiên cứu vẫn mong muốn điều tốt hơn và họ đang đạt được tiến bộ nhanh chóng.
Bước đột phá đầu tiên của lĩnh vực này là cuối năm 2022, Viện Max Planck (CHLB Đức) đã giới thiệu phương pháp MINSTED có thể phân giải các nhãn huỳnh quang riêng lẻ ở độ chính xác gần bằng 1/4 nanomet. Năm 2023, nhóm nghiên cứu thuộc Viện Max Planck tiếp tục cho ra đời phương pháp mới hơn, cung cấp độ phân giải tương đương như khi sử dụng kính hiển vi thông thường, trong đó các phân tử riêng lẻ được dán nhãn bằng các chuỗi DNA riêng biệt. Sau đó, các phân tử này được dò tìm bằng các chuỗi DNA bổ sung được gắn thẻ thuốc nhuộm và chúng liên kết với các mục tiêu tương ứng trong thời gian ngắn nhưng lặp đi lặp lại. Điều này giúp phân biệt các điểm nhấp nháy huỳnh quang riêng lẻ và chúng sẽ mờ thành một đốm màu nếu được chụp ảnh đồng thời. Việc tăng cường độ phân giải bằng phương pháp chụp ảnh tuần tự (RESI - resolution enhancement by sequential imaging) có thể thu được hình ảnh các cặp bazơ riêng lẻ trên một chuỗi DNA, thể hiện độ phân giải ở mức độ ångström (0,1 nanomet) bằng kính hiển vi huỳnh quang tiêu chuẩn.
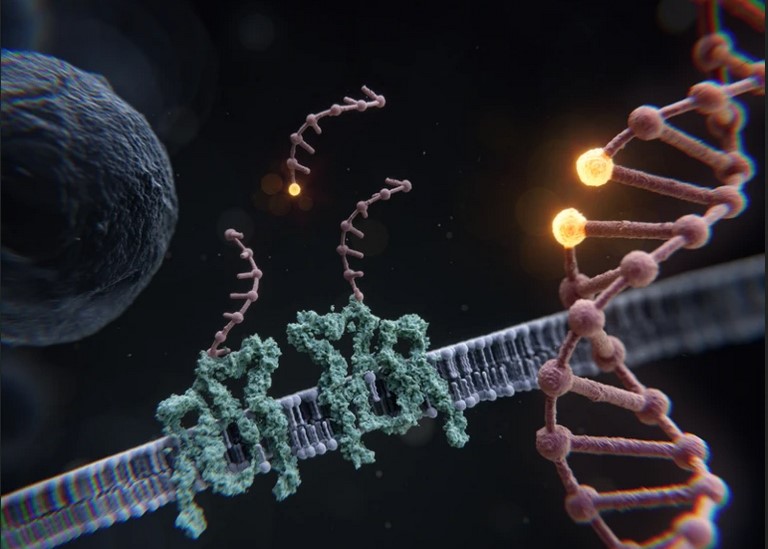
Hình ảnh các cặp bazơ riêng lẻ trong chuỗi DNA được tạo hình bằng công nghệ RESI. Nguồn: Viện Max Planck.
Bên cạnh đó, phương pháp kính hiển vi mở rộng ở kích thước nano một bước (ONE - one-step nanoscale expansion) được phát triển bởi các nhà thần kinh học của Đại học Göttingen (CHLB Đức) cũng giúp mang lại cơ hội chưa từng có để chụp ảnh các cấu trúc tinh tế của từng protein và phức hợp đa protein, cả ở dạng phân lập và trong các tế bào. ONE là phương pháp tiếp cận dựa trên kính hiển vi mở rộng, bao gồm các protein liên kết hóa học trong mẫu với một ma trận hydrogel, phá vỡ các protein và sau đó cho phép hydrogel giãn nở thể tích gấp 1.000 lần. Các mảnh vỡ mở rộng đồng đều theo mọi hướng, bảo toàn cấu trúc protein và cho phép người dùng thu được hình ảnh các đặc điểm cách nhau vài nanomet bằng kính hiển vi đồng tiêu. Phương pháp kính hiển vi ONE có thể cung cấp cái nhìn sâu sắc về các phân tử sinh học có hình dạng linh hoạt hoặc cho phép chẩn đoán trực quan các rối loạn protein cuộn sai như bệnh Parkinson từ các mẫu máu.
Xây dựng các tập bản đồ tế bào
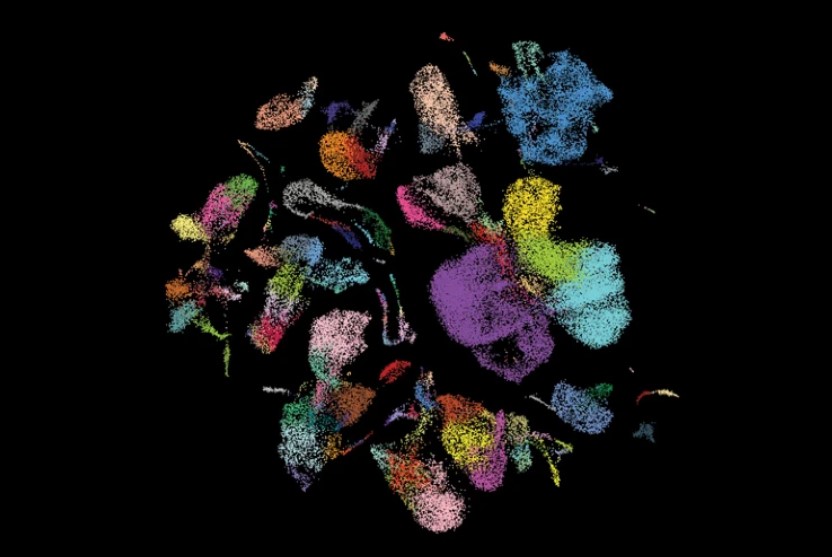
Một tập bản đồ tế bào của phổi người mô tả các loại tế bào khác nhau và cách chúng tác động lẫn nhau. Nguồn Peng He.
Nếu bạn đang tìm kiếm một quán cà phê, các bản đồ trực tuyến có thể giúp bạn tìm thấy những địa điểm gần bạn và cho bạn biết đường đi đến đó. Tuy nhiên, chúng ta chưa có cách nào tương đương để định hướng trong cơ thể phức tạp của con người. Chính vì vậy, các nhà sinh vật học luôn khao khát và nỗ lực xây dựng các bản đồ tế bào. Năm 2016, một dự án bản đồ tế bào người được thực hiện bởi nhà sinh học tế bào Sarah Teichmann tại Viện Wellcome Sanger (Vương quốc Anh), với sự tham gia của khoảng 3.000 nhà khoa học ở gần 100 quốc gia và 10.000 nhà tài trợ. Ngoài ra Viện Y tế Quốc gia Mỹ và Viện Allen (Mỹ) đã tài trợ cho các chương trình về xây dựng bản đồ sinh học phân tử con người, nghiên cứu não bộ thông qua công nghệ thần kinh tiên tiến và mạng lưới điều tra, khảo sát tế bào.
Hoạt động này tiếp tục được thúc đẩy bởi sự phát triển và thương mại hóa nhanh chóng các công cụ phân tích có thể giải mã nội dung phân tử ở cấp độ đơn bào. Ví dụ nền tảng Xenium cho phép khảo sát biểu hiện của khoảng 400 gen cùng một lúc trong 4 mẫu mô mỗi tuần; hay nền tảng PhenoCycler cho phép theo dõi số lượng lớn protein với độ phân giải đơn bào ở định dạng cho phép tái tạo mô 3D. Các phương pháp đa thế hệ khác cho phép các nhà khoa học lập hồ sơ nhiều lớp phân tử trong cùng một tế bào cùng một lúc, bao gồm sự biểu hiện của RNA, cấu trúc của nhiễm sắc thể và sự phân bố protein... Tháng 6/2023, Sarah Teichmann đã công bố một bản phân tích tổng hợp gồm 49 bộ dữ liệu từ phổi của con người, cho biết những thay đổi rõ ràng xảy ra đối với các bệnh như xơ phổi, u phổi hay COVID-19... Vẫn còn rất nhiều công việc phải làm phía trước và ước tính phải mất ít nhất 5 năm nữa dự án bản đồ tế bào người mới hoàn thành. Chúng sẽ có giá trị to lớn trong nhiều lĩnh vực như y tế, chăm sóc sức khỏe, công nghệ gen...
Vật liệu nano in 3D

Các nhà nghiên cứu đã chế tạo được cấu trúc kim loại siêu nhỏ bằng hydrogel. Nguồn: Greer Lab.
Hiện nay việc lắp ráp các cấu trúc nano bằng phương pháp quang polyme hóa nhanh hơn khoảng 3 lần so với các phương pháp in 3D có kích thước nano khác. Tốc độ này có thể đủ tốt để sử dụng trong phòng thí nghiệm, nhưng lại quá chậm đối với các quy trình sản xuất công nghiệp quy mô lớn. Năm 2019, Sourabh Saha, kỹ sư tại Viện Công nghệ Georgia (Mỹ) và các kỹ sư của Đại học Hồng Kông (Trung Quốc) đã chứng minh rằng, họ có thể tăng tốc quá trình trùng hợp bằng cách sử dụng tấm ánh sáng 2D có hoa văn thay vì xung laser thông thường. Điều đó làm tăng tốc độ lên hàng nghìn lần và vẫn có thể duy trì các tính năng ở mức 100 nanomet. Công việc tiếp theo của các nhà nghiên cứu là xác định những con đường mới để chế tạo nano nhanh hơn.
Một thách thức khác là không phải tất cả các vật liệu đều có thể được in trực tiếp thông qua quá trình quang polyme hóa, chẳng hạn như kim loại. Vào năm 2022, các nhà khoa học vật liệu tại Viện Công nghệ California (Mỹ) đã mô tả một phương pháp, trong đó hydrogel được polyme hóa bằng ánh sáng đóng vai trò như một mẫu có kích thước hiển vi, sau đó chúng được trộn với muối kim loại và được xử lý theo cách khiến kim loại đảm nhận cấu trúc của mẫu đồng thời co lại. Với kỹ thuật này, các nhà nghiên cứu rất tin tưởng vào tiềm năng chế tạo các cấu trúc nano chức năng từ các kim loại và hợp kim chắc chắn, có nhiệt độ nóng chảy cao.
Một rào cản quan trọng là các hệ thống dựa trên xung laser được sử dụng trong nhiều phương pháp quang polyme hóa có giá lên tới 500.000 USD, nhưng những lựa chọn thay thế rẻ hơn đang xuất hiện. Nhà vật lý Martin Wegener và các đồng nghiệp tại Viện Công nghệ Karlsruhe (CHLB Đức) đã khám phá ra các tia laser liên tục rẻ hơn, nhỏ gọn hơn và tiêu thụ ít năng lượng hơn so với các tia laser xung tiêu chuẩn. Ông đã thành lập một công ty khởi nghiệp nhằm thương mại hóa quy trình chế tạo các tấm kim loại có cấu trúc nano, phù hợp cho các ứng dụng như áo giáp thế hệ mới hoặc các lớp bên ngoài siêu bền và chống va đập cho máy bay và các phương tiện khác.
Nhật Nam (theo Nature)