Các ứng dụng đo lường linh hoạt với kỹ thuật SPR
SPR là một công cụ mới trong nghiên cứu về tương tác liên kết của phối tử (ligand) với các protein màng - là đích tác động chính của thuốc sinh học. Trong kỹ thuật SPR, một chất tham gia tương tác được cố định vào bề mặt cảm biến, chất còn lại được giữ tự do trong dung dịch và được bơm qua bề mặt này. Sự liên hợp và phân ly của hai phân tử được đo đạc và hiển thị dưới dạng một biểu đồ. Các ứng dụng đo lường phổ biến của SPR gồm:
Xác định độ đặc hiệu: một chất cần phân tích được đưa vào bề mặt cảm biến, sau một khoảng thời gian nhất định, phản ứng/đáp ứng sẽ được đo. Vẽ đường cong đáp ứng tương quan giữa các mẫu sẽ chỉ ra được độ bền tương đối của liên kết. Tín hiệu nền sinh ra bởi dung môi hòa tan chất phân tích sẽ được bù trừ nhờ vào một buồng đo tham chiếu.
Nồng độ của một chất phân tích được đo bằng cách sử dụng bề mặt cảm biến có mật độ phối tử rất cao. Tốc độ liên hợp của chất phân tích với phối tử trên bề mặt cảm biến này sẽ tỷ lệ với nồng độ của chất đó. Sau khi dựng được đường chuẩn với các nồng độ khác nhau, các mẫu chưa biết nồng độ có thể được đo nhanh chóng.
Xác định độ bền của liên kết: có hai cách để xác định độ bền của liên kết. Cách thứ nhất, sử dụng nhiều nồng độ chất phân tích được bơm qua phối tử cho đến khi đạt tín hiệu tương hợp và phân ly cân bằng nhau. Bằng cách vẽ đường cong đáp ứng tối đa tương ứng với mỗi nồng độ, ta thu được một hàm số để ước tính hằng số ái lực của tương tác (KD). Cách thứ hai, ủ hai chất tương tác với nhau và chờ cho đến khi cân bằng. Nồng độ một chất tương tác được giữ không đổi và thay đổi nhiều nồng độ cho chất còn lại. Nạp hỗn hợp này vào hệ thống SPR sẽ giúp xác định nồng độ của chất phân tích tự do sau khi tương tác đã cân bằng.
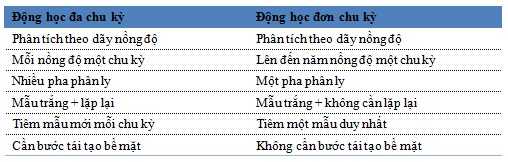
Đánh giá tính chất của hệ tương tác: động học tương tác giúp mô tả tương tác giữa một hay nhiều chất phân tích. Sau khi tương tác với nhau, các chất phân tích và phối tử tách nhau ra mà không làm biến đổi lẫn nhau, trái ngược với động học enzym. Tốc độ liên hợp được xác định theo thời gian thực khi chất phân tích chảy qua bề mặt phối tử. Theo thời gian, dung môi sẽ cuốn trôi chất phân tích, từ đó tốc độ phân ly có thể được ghi nhận. Toàn bộ đường cong liên hợp và phân ly lúc này được gán vào một mô hình động học có sẵn để đánh giá. Nếu kết quả khớp với mô hình, hằng số cân bằng sẽ được tính toán và hiển thị. Có 2 phương pháp tiếp cận thực nghiệm cho thí nghiệm động học, gồm: đa chu kỳ (cách tiếp cận “tiêu chuẩn” truyền thống) và đơn chu kỳ (bảng 1).
Bảng 1. Các chiến lược bơm mẫu khác nhau giữa phân tích động học tương tác đơn chu kỳ và đa chu kỳ giữa phối tử và chất cần phân tích.
Nghiên cứu ái lực cấu trúc - chức năng: chức năng được đo lường bằng độ đặc hiệu (ái lực), tốc độ và hằng số cân bằng, cũng như đặc tính nhiệt động lực học. Trong phần lớn các thử nghiệm với SPR, điều kiện tương tác sẽ được giữ ổn định, việc chủ động thay đổi những điều kiện này (ví dụ: nhiệt độ) có thể tiết lộ những đặc tính nhiệt động lực học quan trọng. Hệ thống SPR có thể đo lường được các tương tác đặc hiệu này giữa phối tử và chất phân tích theo thời gian thực, cho phép các nhà nghiên cứu cùng lúc ước lượng được cả tốc độ và hằng số cân bằng.
Phương pháp phân tích nồng độ không cần đường chuẩn (CFCA) đã được phát triển thêm để đo nồng độ các phối tử đang thực sự có hoạt tính. Phương pháp dựa trên giới hạn vận chuyển khối lượng, hiện tượng xuất hiện khi sử dụng bề mặt phối tử mật độ cao. Bằng cách bơm chất phân tích với hai tốc độ dòng khác nhau (ví dụ: 10-90 µl/phút), nồng độ chất phân tích đang thực sự có hoạt tính có thể được tính toán từ độ dốc của các đường cong đáp ứng ghi nhận được.
Phân tích đặc tính và so sánh các thuốc sinh học bằng SPR
Thuốc sinh học là các sản phẩm phức tạp, do đó cần xác định đặc tính bằng nhiều công cụ phân tích nhằm bổ sung cho nhau. Thuốc tương tự sinh học (Biosimilar) là sản phẩm tương tự về chất lượng, an toàn và hiệu quả với một sản phẩm trị liệu sinh học tham chiếu đã được cấp phép lưu hành. Do vậy, thuốc tương tự sinh học chỉ cần một số thử nghiệm lâm sàng tối giản trước khi được cấp phép lưu hành với điều kiện nó đã được chứng minh so sánh với sản phẩm gốc tương ứng bằng các thử nghiệm phân tích đặc tính nghiêm ngặt. Các thử nghiệm so sánh này cũng dựa trên một nền tảng nhiều công cụ phân tích nhằm bổ sung cho nhau (hình 1). Nếu không chứng minh được tính tương tự của sản phẩm sẽ dẫn đến phát sinh chi phí đáng kể cho thử nghiệm lâm sàng nghiêm ngặt hơn để nhận được sự phê duyệt của cơ quan quản lý. Các tài liệu hướng dẫn từ các cơ quan quản lý y tế như FDA và EMA, đặc biệt nhấn mạnh tầm quan trọng của các phân tích đặc tính nghiêm ngặt này trong việc chỉ ra sự tương tự giữa một thuốc tương tự sinh học và thuốc gốc dựa trên các đánh giá toàn diện nhất về chức năng lẫn cấu trúc protein. Do đó, các nhà phát triển thuốc sinh học cần sử dụng một bộ công cụ với các công nghệ hiện đại nhất để phân tích, đánh giá. Các công ty như Sandoz và Celltrion đều đã có những thuốc sinh học tương tự được FDA phê duyệt, đã thành công trong việc sử dụng các phân tích lý sinh theo thời gian thực, không đánh dấu như là một cách tiếp cận nền tảng trong quy trình phát triển sản phẩm, đánh giá tương tác giữa phân tử đích và thụ thể, đo đặc tính sinh miễn dịch và độ đặc hiệu.
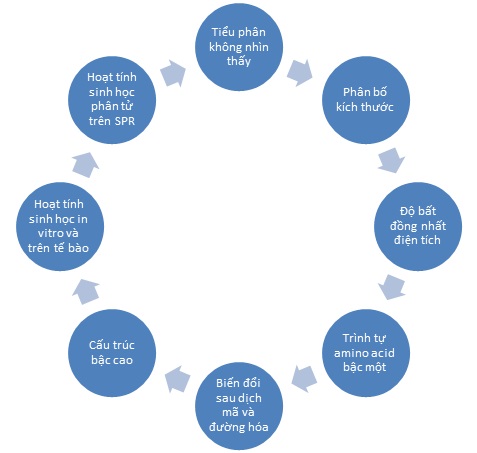
Hình 1. Các đặc tính cần phân tích và kiểm soát trong quá trình phát triển thuốc tương tự sinh học.
Một thách thức đáng kể khác với thuốc tương tự sinh học cũng như các sản phẩm sinh học khác là việc chuẩn hóa các tương tác với thụ thể Fc. Các thụ thể này có thể được dùng như chất kích hoạt, ức chế, hoặc không có bất kỳ tác dụng nào đến cơ chế đáp ứng gây độc tế bào phụ thuộc kháng thể (ADCC) hay bổ thể (CDC). Tuy nhiên, xác định đặc tính và sự tương tác của những sản phẩm phức tạp này là cực kỳ khó khăn.
Kháng thể đơn dòng (mAb) hiện nay đang là nhóm thuốc sinh học phát triển nhanh nhất và đã được chứng minh thành công trong việc điều trị rất nhiều loại bệnh như nhóm các bệnh ung thư, tự miễn và truyền nhiễm. Kháng thể nhận biết kháng nguyên qua vùng biến đổi (Fv) trong phần liên kết kháng nguyên (Fab). Kết quả là chúng có thể can thiệp vào chức năng của kháng nguyên, cho ra hiệu ứng trị liệu. Mặt khác, qua vùng hằng định (Fc), chúng có thể tương tác được với các phân tử liên kết Fc rồi thu hút các thành tố miễn dịch của bệnh nhân đến để phá hủy mục tiêu được chỉ định. Đáp ứng ADCC được kích hoạt bởi một tương tác giữa vùng Fc và một kháng thể gắn vào nó, ví dụ, một tế bào khối u và các thụ thể Fcγ trên tế bào chức năng miễn dịch khi được kích hoạt sẽ giúp loại bỏ tế bào u bằng thực bào hay tan bào (phụ thuộc vào loại tế bào chức năng ở trên). Đáp ứng CDC bắt đầu bởi thành phần bổ thể C1q liên kết với vùng Fc của kháng thể, gây ra sự hoạt hóa bổ thể và tiêu diệt tế bào mục tiêu bằng thực bào, tan bào, hay phá vỡ màng tế bào.
SPR là một kỹ thuật được xây dựng và tối ưu để phát hiện cũng như theo dõi tương tác phân tử sinh học theo thời gian thực. Nhiều nhà nghiên cứu đã thu nhận kết quả với độ chính xác, độ lặp lại và tuyến tính rất cao, giúp SPR trở thành công cụ hữu ích cho việc so sánh, ước tính hiệu lực và kiểm tra tính ổn định của thuốc sinh học. SPR cũng thể hiện độ chính xác và độ lặp lại cao hơn so với các phương pháp thử nghiệm trên tế bào truyền thống như đánh giá ADCC và CDC.
Các ứng dụng của SPR không chỉ giới hạn ở các phân tích động học tương tác phối tử - thụ thể mà còn được sử dụng trong sàng lọc và phát triển thuốc. Có nhiều dạng cảm biến sinh học SPR khác nhau (dạng mảng, đa kênh, hình ảnh), cho phép phát hiện và phân tích liên tục hàng trăm đến hàng nghìn sự kiện liên kết ái lực trên bề mặt chip. Trong kỹ thuật SPR hình ảnh, góc tới được giữ cố định và tương tác của các phân tử sinh học trên bề mặt vàng được đo đạc bởi sự thay đổi cường độ tia phản xạ, khác với các cảm biến SPR khác vốn theo dõi sự thay đổi của góc hấp phụ hay bước sóng tia phản xạ. Mặc dù có nhiều ưu điểm và lợi ích nhưng các cảm biến sinh học SPR thông thường cũng có hạn chế là không hỗ trợ phân tích đa mục tiêu (multiplexing). Ngược lại, công nghệ SPR hình ảnh sử dụng cảm biến sinh học hỗ trợ nhiều chất phân tích giúp gia tăng thông lượng nhưng vẫn đạt được độ nhạy tương đương với cảm biến SPR thông thường. Do đó, các hệ thống SPR hình ảnh không yêu cầu đánh dấu sẽ thích hợp hơn cho sàng lọc thông lượng cao (HTS), đặc biệt trong sàng lọc thuốc, hơn bất kỳ kỹ thuật phát hiện nào dựa trên quang học.
Các ứng dụng của SPR cho kháng thể thường được chia thành hai loại là sàng lọc và phân tích đặc tính. Sàng lọc kháng thể diễn ra bằng việc gắn các kháng thể lên bề mặt chip rồi tiêm vào kháng nguyên tương ứng. Động học của liên kết có thể ước lượng trực tiếp từ thí nghiệm sàng lọc và là thông số được quan tâm chính khi tìm kiếm các kháng thể với mục đích sử dụng cho chẩn đoán và điều trị. Kháng thể với tốc độ phân ly chậm thường được lựa chọn là ứng viên cho các thuốc cần thời gian lưu kéo dài và có tiềm năng cho hiệu quả điều trị cao hơn. Một yếu tố cũng làm việc lựa chọn ứng viên trở nên phức tạp là độ đặc hiệu của liên kết, các kháng thể đa mục tiêu cũng thường bị loại bỏ và thay bằng các ứng viên có độ đặc hiệu cao hơn. Do đó, việc lựa chọn ứng viên thuốc không chỉ dựa trên các liên kết ổn định mà còn phải đặc hiệu. Trong các thử nghiệm phân tích đặc tính kháng thể, SPR thường được sử dụng để đánh giá khả năng liên kết với epitope, độ đặc hiệu, nồng độ và ái lực/động học. Khi sử dụng SPR cho việc lập hồ sơ so sánh thuốc, sản phẩm sinh học tương tự cũng sẽ được so sánh với sản phẩm gốc về các tiêu chí vừa liệt kê.
Nghiên cứu điển hình
Kháng thể, cytokine và hormone thường tương tác với các thụ thể của chúng. Trong khi cytokine và hormone thường bảo tồn sự gấp cuộn và trình tự tự nhiên của chúng, các kháng thể trị liệu được chủ động thiết kế để tương tác với phân tử đích của chúng (bao gồm kháng nguyên, thụ thể Fc và các thành phần bổ thể) dựa trên cơ chế tác dụng mà nhà phát triển hướng đến.
Trong một nghiên cứu phân tích động học liên kết của các thuốc sinh học tương tự rituximab và ristova với thụ thể FcRγIIIa (Cd16a), phân tích động học của liên kết với FcRγIIIa (Cd16a) được thực hiện bằng cách tiêm nhiều nồng độ khác nhau của thuốc kháng thể cần phân tích (từ 0,25 đến 4 µM) được thực hiện trên phệ thống phân tích Biacore (Cytiva) với thiết kế thí nghiệm như hình dưới đây.
-2.jpg)
Hệ thống SPR giúp đưa ra sự so sánh trực quan về động học liên kết của các thuốc sinh học tương tự rituximab với thụ thể FcγRIIIa người khi so sánh trực tiếp với thuốc gốc Ristova. Như đã thấy trên bảng 2, giá trị KD của thuốc sinh học tương tự rituximab với FcγRIIIa được ghi nhận với cùng độ chia của thuốc Ristova. Các giá trị KD đo được cho thấy Ristova thể hiện ái lực liên kết lớn hơn các thuốc sinh học tương tự rituximab khác. Chỉ ứng viên thuốc sinh học tương tự số hai là cho thấy ái lực với liên kết FcγRIIIa có thể cạnh tranh được với Ristova.
-1.jpg)
Thay lời kết
SPR là một kỹ thuật đã và đang được phát triển nhanh chóng để sử dụng trong các phân tích tương tác protein cũng như sàng lọc lựa chọn kháng thể hay ứng viên thuốc phân tử nhỏ dựa trên các đặc tính tương tác mong muốn. Khi cần phân tích đặc tính tương tác của một cặp phân tử, toàn bộ dữ liệu thu nhận từ đường cong đáp ứng sẽ được gán với một mô hình tương tác lý thuyết, nếu phù hợp, sẽ tính toán được ái lực và các hệ số động học đại diện cho tương tác đang quan tâm. Trong đó, giá trị đáp ứng giúp xác nhận tương tác bám có xảy ra hay không và độ ổn định của tương tác này sẽ được dùng làm cơ sở để so sánh và sàng lọc kết quả. Đây là một kỹ thuật thông lượng cao có thể được sử dụng làm công cụ hữu ích để đánh giá mức độ toàn vẹn của protein ở cấu trúc bậc cao nhằm so sánh cũng như phân tích đặc tính của các protein này. Kết quả cho thấy, kỹ thuật SPR mang đến một cái nhìn sâu sắc hơn trong việc phân tích đặc tính và so sánh các thuốc sinh học, thuốc tương tự sinh học trên thị trường với nhau.
Phạm Minh Vũ
(Lược dịch theo Biopharm International)