Vai trò của di truyền trong ung thư
Một số đột biến ảnh hưởng tới chức năng bình thường của gen ức chế khối u, điều hoà tăng trưởng và chết tế bào thường có khả năng bảo vệ cơ thể, chống lại ung thư. Đột biến các gen ức chế khối u, ví dụ như BRCA1 và BRCA2 được chứng minh là tăng nguy cơ ung thư vú, buồng trứng và tuyến tiền liệt. Một số đột biến di truyền tác động đến khả năng sửa chữa DNA của tế bào cũng có thể dẫn tới ung thư, ví dụ như ung thư vú có đột biến trên gen HER2 liên quan tới sản xuất một loại protein tăng trưởng tế bào ung thư. Trong một số trường hợp, đột biến có thể di truyền tới đời sau như BRCA1 và BRCA2, nhưng hầu hết các đột biến không có tính di truyền.
Xét nghiệm đột biến được coi là cần thiết trong điều trị ung thư. Vào năm 2018, một nghiên cứu đã phát hiện ra 4 nhóm đột biến khác nhau trên u lympho tế bào B lớn lan toả, mỗi nhóm đột biến có biểu hiện lâm sàng, tiến triển và đáp ứng điều trị khác nhau. Do đó chẩn đoán đúng đột biến vô cùng quan trọng để có điều trị phù hợp.
Một vài đột biến di truyền có thể ảnh hưởng mạnh mẽ tới điều trị, thậm chí cả khi điều trị không thực sự tác động trực tiếp tới đột biến. Ví dụ như, trong bệnh bạch cầu mạn tính dòng lympho (chronic lymphocytic leukemia), khi bệnh nhân có đột biến gen TP53 nghĩa là ung thư có khả năng không đáp ứng với điều trị hoá miễn dịch. Nếu bác sĩ điều trị biết được bệnh nhân có đột biến gen này thì có thể lựa chọn phương pháp điều trị khác tốt hơn như ghép tế bào gốc. Một trường hợp khác trong ung thư đại trực tràng, đột biến gen KRAS đồng nghĩa với bệnh nhân không đáp ứng với cetuximuab hoặc panitumumab. Trong ung thư, một vài đột biến có thể là tín hiệu gợi ý rằng loại ung thư đó có nguy cơ kháng một số điều trị tương ứng.
Giải trình tự gen ung thư
Giải trình tự bộ gen ở những bệnh nhân ung thư không chỉ nhằm mục đích tìm ra đột biến có thể điều trị được, mà còn là để xác định những đột biến không điều trị được hoặc đánh giá điều trị của từng loại thuốc khác nhau. Xác định đột biến của bệnh nhân để xác định phương pháp điều trị phù hợp, hoặc ngay cả khi đột biến đó không thể hỗ trợ lựa chọn phương pháp điều trị phù hợp, thì những thông tin liên quan như tiên lượng bệnh cũng rất đáng giá.
Chương trình thành lập hệ gen ung thư (The Cancer Genome Atlas programme) được Viện Ung thư quốc gia Mỹ (NCI)) khởi động, đã giải trình tự cho hơn 20.000 bệnh nhân có ung thư tiên phát, trải rộng tới 33 loại ung thư khác nhau.
Bên cạnh giải trình tự gen, những kỹ thuật mới hơn cũng mang lại số lượng thông tin quý giá để xác định đặc tính và điều trị ung thư, ví dụ như giải trình tự RNA, biểu hiện gen và proteomics. Cùng lúc đó, một số phương pháp điều trị như ức chế điểm kiểm soát và liệu pháp miễn dịch đang vượt xa điều trị dựa trên hệ gen ung thư. Những phương pháp này nhắm tới những ung thư ức chế đáp ứng miễn dịch tế bào, từ đó xác định và tiêu diệt tế bào ung thư.
Vào nửa sau của thế kỷ XX, các nhà khoa học nghiên cứu cấu trúc của chromosome ở tế bào mang bệnh và phát hiện ra nhiễm sắc thể bất thường (Philadelphia chromosome) có liên hệ với bệnh bạch cầu mạn dòng tuỷ (CML). Sau đó là phát hiện nhiễm sắc thể có khả năng chuyển đoạn không tương hỗ. Vào năm 2004, phương pháp giải trình tự gen thế hệ mới đã hé mở những thông tin về các đột biến quan trọng trong ung thư như đột biến trên PIK3CA và ECFR.
Khi Dự án về Hệ gen người (Human Genome Project) được hoàn thành năm 2003, các nhà khoa học đã kỳ vọng về tính khả thi của việc giải trình tự hệ gen ung thư. Dù vậy, có một vài khó khăn cần phải vượt qua, bao gồm cả kinh phí đáng kể để giải trình tự hệ gen ung thư, và cần có một công cụ phân tích phù hợp cho hệ gen cũng như cho đột biến soma.
Tiến bộ mới nhất trong giải trình tự gen ung thư
Tác giả T.J Ley và cs (2008) [1] đã lần đầu tiên công bố trình tự gen của ung thư ở bệnh nhân có bệnh bạch cầu cấp dòng tuỷ (AML) (hình 1).
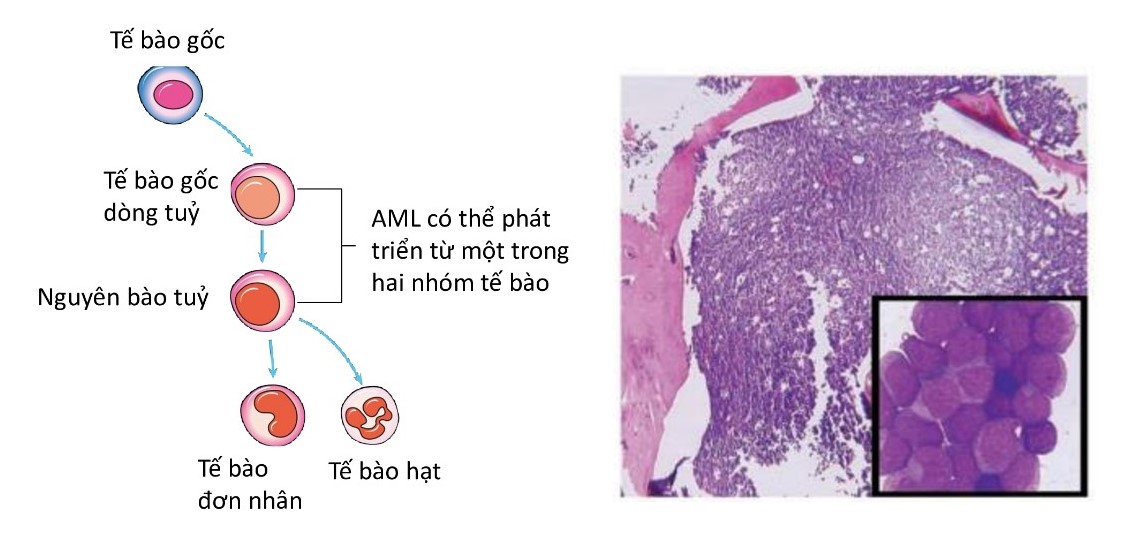
Hình 1. Nguồn gốc bệnh bạch cầu cấp dòng tủy và mẫu sinh thiết tủy xương ở một bệnh nhân với các hình ảnh tăng mật độ tế bào (>90%) toàn bộ là nguyên bào tủy chưa trưởng thành.
Bộ dữ liệu hệ gen này đã phần nào hé mở những ẩn số về đặc điểm sinh học ung thư và điều trị ung thư. Nghiên cứu này đòi hỏi quy trình phân tích nghiêm ngặt dữ liệu gen có nguồn gốc từ các tế bào không phải khối u của bệnh nhân, có thể lấy từ da, để loại ra những đột biến không liên quan tới ung thư - những đột biến đơn độc (germline polymorphisms) hoặc những đột biến xảy ra trong ung thư nhưng là đột biến “đi kèm” (passenger mutation) và không là nguyên nhân gây ra ung thư (hình 2).

Hình 2. Sơ đồ khái quát 15 năm nhìn lại những phát hiện về hệ gen ung thư.
Nếu không có bộ dữ liệu hệ gen bình thường và ung thư, có lẽ rất khó để lọc ra được những đột biến gây bệnh trong số 3,8 triệu đột biến trong hệ gen. Nhóm nghiên cứu đã tìm ra được 10 gen cần thiết để dẫn tới AML, trong số đó có 2 gen đã được báo cáo trước đây là có liên quan tới tiến triển ung thư và 8 gen mới, tuy nhiên chức năng của 8 gen này trong tế bào ung thư vẫn chưa được làm rõ. Một phương pháp quan trọng để đánh giá tần số xuất hiện tương đối của đột biến trong hệ gen của một cá nhân trong quần thể mang gen ung thư khác nhau được gọi là read-count data (tạm dịch: số lần đọc). Bằng cách tận dụng dữ liệu ghi nhận số lần đọc, nhóm nghiên cứu có thể suy ra tần số “đọc” đột biến tại một vị trí cụ thể trong bộ gen và thu được một giá trị gọi là tần số alen đột biến (VAF). VAF đưa ra những gợi ý về các dòng tế bào có liên quan tới ung thư tiềm ẩn trong mẫu bệnh phẩm, từ đó thúc đẩy kháng điều trị hoặc biến thể mới của bệnh. Những suy luận trên đã được chứng minh là đúng bằng phương pháp giải trình tự DNA đơn bào (single-cell DNA sequencing). Tuy vậy T.J. Ley và cs (2008) [1] nhấn mạnh rằng, bộ gen nên được giải trình tự với quy mô lớn hơn trong tương lai.
Một điểm khác đáng chú ý là, trong một nghiên cứu tiếp theo trên bộ gen lớn hơn của AML, tác giả T.J. Ley và cs (2008) [1] đã phát hiện luôn có sự hiện hiện của đột biến gen IDH1. Liên hệ với bài nghiên cứu giải trình tự vùng mã hoá protein của hệ gen ở ung thư não, xác nhận được gen IDH1 gây một loại ung thư não tên là glioma. Nghiên cứu này là tiền đề cho nghiên cứu về cơ chế và điều trị tìm hiểu đột biến của protein IDH1 và IDH2 sản xuất ra phân tử thúc đẩy ung thư 2-hydroxyglutarate. Loại protein đột biến này có thể điều trị mục tiêu nhằm mang lại lợi ích lâm sàng trong ung thư não và AML. Những phát hiện này cho thấy nghiên cứu về hệ gen có thể xác định những đột biến mà trước đây chúng ta chưa biết, kèm với tiên lượng, kết cục điều trị.
Với xu hướng giảm kinh phí trong giải trình tự gen và ngày càng có nhiều hợp tác quốc tế tập trung vào hệ gen ung thư hơn, mảng nghiên cứu hệ gen ung thư đã xác định được 3 triệu biến đổi gen trong hàng chục nghìn bộ gen ung thư ở người, trải rộng trên hàng chục phân nhóm ung thư, với tác động cơ học và điều trị ngày càng tăng. Các nhà khoa học tiếp tục những nghiên cứu sâu hơn về giải trình tự gen tế bào đơn độc cũng như trên các nhóm dân số lớn hơn.
Ngày nay, giải trình tự hệ gen giống như một phần gắn liền với lâm sàng, thay đổi chẩn đoán ung thư, các thử nghiệm lâm sàng và sử dụng những phương pháp điều trị mới nhằm cải thiện kết quả điều trị ở bệnh nhân ung thư. Những kết quả nghiên cứu mới nhất về bộ gen ung thư cung cấp thông tin cho các bác sĩ lâm sàng và các nhà khoa học xác định được mối liên quan của nhóm người mắc bệnh ung thư về mặt sinh học, bộ gen và cuối cùng là xác định các phương pháp điều trị và dấu ấn sinh học mới. Kết quả nghiên cứu cũng cung cấp một lăng kính quan trọng để nghiên cứu và thẩm vấn các tình trạng tiền ác tính, trong đó các mô có thể có thể khảm (moisacism) và các tế bào chứa đột biến liên quan đến ung thư.
TÀI LIỆU THAM KHẢO
[1] T.J. Ley, E.R. Mardis, L. Ding, et al. (2008), "DNA sequencing of a cytogenetically normal acute myeloid leukaemia genome", Nature, 456(7218), pp.66-72, DOI: 10.1038/nature07485.
[2] B. Nogrady (2020), “How cancer genomics is transforming diagnosis and treatment”, Nature, 579(7800), pp.S10-S11, DOI: 10.1038/d41586-020-00845-4.
[3] S.F. Cai, R.L. Levine (2023), “15 years after a giant leap for cancer genomics”, Nature, 623(7989), pp.920-921, DOI: 10.1038/d41586-023-03626-x.