Định hướng phát triển lớp phủ kháng virus SARS-CoV-2
Khởi nguồn tại thành phố Vũ Hán từ cuối tháng 12/2019, đại dịch COVID-19 với tác nhân là virus SARS-CoV-2 (hình 1) đã lan rộng gần như khắp thế giới, gây ra bệnh tật và tử vong đối với con người, kéo theo sự khủng hoảng kinh tế - xã hội của nhân loại. Theo nhiều báo cáo khoa học gần đây, virus SARS-CoV-2 có thể tồn tại lên đến một tuần trên bề mặt của nhiều vật liệu rắn [1, 2]. Điều này gây ra nguy cơ lây nhiễm tiềm ẩn rất đáng lo ngại khi con người vô tình tiếp xúc với các bề mặt vật dụng công cộng, chẳng hạn như tay nắm cửa, nút bấm trên máy rút tiền ATM hay vỏ điện thoại di động… Chính vì vậy, nhiều nhà khoa học cho rằng, một trong những phương pháp góp phần giúp hạn chế mức độ lây lan của virus này là tìm cách giảm thiểu thời gian sống của chúng trên bề mặt vật liệu. Xuất phát từ quan điểm trên, nhóm nghiên cứu của GS William A. Ducker (Khoa Kỹ thuật hóa học và vật lý sinh học, Đại học Virginia Tech, Hoa Kỳ) đã tiến hành nghiên cứu tổng hợp lớp phủ có khả năng kháng virus SARS-CoV-2. Cụ thể, lớp phủ này phải có khả năng: (i) ức chế hoạt động của virus một cách nhanh chóng, (ii) dễ dàng được phủ lên nhiệt bề mặt rắn khác nhau và (iii) đủ mạnh để duy trì khả năng kháng virus trong thời gian sử dụng. Khi đó, lớp phủ có thể được ứng dụng không chỉ cho đồ gia dụng mà còn cho các vật liệu y tế, thương mại…

Hình 1. Ảnh minh họa virus SARS-CoV-2.
Tuy nhiên, cho đến hiện tại, các nhà khoa học vẫn chưa biết các nhóm hợp chất nào có khả năng ức chế SARS-CoV-2. Do đó, GS William A. Ducker và cộng sự đã thử nghiệm trên một số màng mỏng có bản chất là các đơn lớp polymer cationic. Những màng mỏng này được mong chờ có thể giúp ức chế mầm bệnh hiệu quả nhờ sở hữu mật độ điện tích cao, có khả năng làm gián đoạn quá trình tự lắp ráp của nhiều loại virus và vi khuẩn [3, 4]. Đáng tiếc, đối với virus SARS-CoV-2, kết quả thử nghiệm không được như mong đợi.
Đặc tính kháng virus của Cu2O
Kết quả trên thúc đẩy nhóm nghiên cứu tiến hành thử nghiệm trên nhiều loại vật liệu màng mỏng khác nhau. Một số nghiên cứu trước đó đã chỉ ra SARS-CoV-2 có thời gian sống ngắn trên bề mặt kim loại đồng [1], khi mà nhiều lớp nguyên tử Cu trên bề mặt dễ dàng bị oxy hóa thành Cu2O. Từ lâu, Cu2O đã được sử dụng như một chất hoạt tính trong thuốc trừ sâu và được xếp vào nhóm độc chất thứ III bởi Cơ quan Bảo vệ môi trường (EPA), tương ứng với các hợp chất gây độc nhẹ [5]. Oxit này còn được sử dụng trong sơn vỏ tàu biển nhờ đặc tính ngăn ngừa sự bám dính và làm chậm sự phát triển của các sinh vật biển trên vỏ tàu [6, 7]. Điều thú vị là trong một nghiên cứu lâm sàng gần đây, Cu2O được báo cáo không gây tác hại nào đáng kể trên da người [8]. Ngoài ra, theo báo cáo của EPA năm 2009, lượng Cu trong thuốc trừ sâu cũng không cho thấy nguy cơ nào đối với cộng đồng. Phản ứng miễn dịch của cơ thể đối với Cu cũng rất hiếm, bất chấp việc tiếp xúc với đồng tiền bằng Cu diễn ra thường xuyên ở nhiều đất nước.
Chính vì vậy, nhóm nghiên cứu của GS Ducker đã đề nghị tổng hợp hệ vật liệu dạng composite với các hạt Cu2O được phân tán đều trong màng mỏng polyurethane (PU, dày 10-16 μm) thông qua phương pháp quét phủ đơn giản. Hệ vật liệu này sau đó sẽ được kiểm tra đặc tính kháng virus với SARS-CoV-2 cô lập từ Hong Kong.
Tổng hợp màng mỏng Cu2O/PU
Quy trình chế tạo màng mỏng Cu2O/PU được thực hiện qua 3 giai đoạn. Đầu tiên, một lớp rất mỏng PU được quét phủ lên bề mặt kính rồi để khô trong vòng 8 phút để đóng rắn một phần. Tại thời điểm này, polymer vẫn còn lỏng đủ để gần như không lưu dấu khi dùng tay chạm vào. Mặt khác, hệ huyền phù Cu2O (10% khối lượng) trong ethanol được chuẩn bị và đánh siêu âm trong 3 phút. Sau đó 1 ml huyền phù được phủ lên lớp phim PU, để khô trong 5 phút ở nhiệt độ phòng. Đến giai đoạn thứ 2, lớp màng mỏng được nung trong lò ở 120oC trong 2 giờ để hoàn tất quá trình đóng rắn, rồi được thổi mạnh với N2 nén, rửa với nước khử ion và sấy khô trong khí quyển N2. Ở giai đoạn cuối, mẫu được đặt vào buồng chân không, thổi khí argon trong 10 phút rồi trải qua quá trình xử lý với plasma argon trong 3 phút ở công suất 100 W và áp suất nhỏ hơn 200 mTorr nhằm loại bỏ phần PU dư.
Hình 2 thể hiện ảnh kính hiển vi điện tử (chụp bề mặt (A) và mặt cắt ngang (B) của mẫu Cu2O/PU. Dễ dàng nhận thấy, vật liệu màng phủ có bề mặt gồ ghề với các hạt Cu2O đa diện, phân bố ngẫu nhiên. Các hạt này có kích thước dao động từ 100 đến 200 nm và chồng lấp lên nhau, tạo thành màng phim với độ dày trong khoảng 10-16 μm.

Hình 2. Ảnh kính hiển vi điện tử quét của vật liệu màng mỏng Cu2O/PU: (A) Chụp bề mặt và (B) Mặt cắt ngang.
Thành phần nguyên tố được kiểm định thông qua phổ quang điện tử tia X (XPS). Cụ thể, phổ XPS Cu 2p (hình 3A) cho thấy một peak Cu 2p3/2 cường độ cao định vị tại 932,7 eV, vốn là năng lượng liên kết đặc trưng của Cu2O. Tỷ lệ hợp thức của oxit đồng có thể được kiểm tra từ tỷ lệ diện tích giữa các peak O 1s (hình 3B) và Cu 2p. Theo đó, tỷ lệ O/Cu đạt giá trị 1,8:1, khá gần với tỷ lệ hợp thức của Cu2O. Kết quả này chứng tỏ phương pháp quét phủ rồi xử lý với plasma Ar không ảnh hưởng nhiều đến môi trường hóa học của các hạt Cu2O cũng như cản trở sự phân bố hạt Cu2O trong màng phim PU.
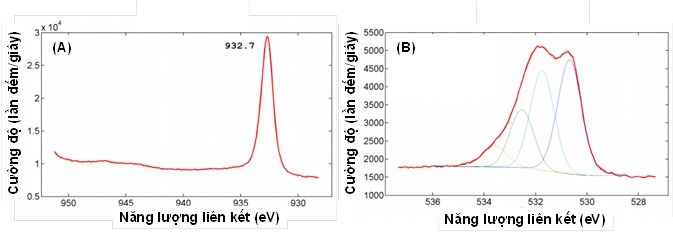
Hình 3. Phổ XPS của mẫu Cu2O/PU: (A) Vùng Cu 2p, (B) Vùng O 1s.
Khảo sát khả năng ức chế virus SARS-CoV-2 của màng mỏng Cu2O/PU
Để có thể khảo sát khả năng kháng virus SARS-CoV-2, nhóm nghiên cứu áp dụng phương pháp của Chin và cộng sự [2]. Cụ thể, trước khi tiếp xúc với virus, màng mỏng Cu2O/PU được khử trùng với dung dịch ethanol 70%, làm khô ở 37oC qua đêm. Virus SARS-CoV-2 sau khi cô lập sẽ được nuôi bởi tế bào Vero E6 trong môi trường Eagle bổ sung 2% huyết thanh bào thai bò và 1% penicillin-streptomycin ở 37°C. Tiếp theo, 5 μl dung dịch chứa 6,2×107 (107,8) TCID50/ml SARS-CoV-2 được nhỏ lên bề mặt lớp phủ với độ ẩm 60-70% ở 22-23oC rồi làm khô ở khoảng 30 phút. Sau một thời gian nhất định, vật liệu phủ Cu2O/PU được ngâm trong 300 μl dung dịch Eagle bổ sung 0,5% albumin huyết thanh bò và 0,1% glucose, pH 7,4 ở nhiệt độ phòng để pha loãng virus. Lượng virus này được xác định bằng thực nghiệm đo TCID50 (lượng gây chết 50% tế bào) trong tế bào Vero E6.
Kết quả so sánh giữa tấm kính không phủ và có phủ Cu2O/PU cho thấy quá trình ức chế virus bằng lớp phủ Cu2O/PU diễn ra rất ấn tượng: gần 99,99% virus bị tiêu diệt trên bề mặt Cu2O/PU chỉ trong vòng 1 giờ (hình 4), ngược lại, lượng virus giảm trên bề mặt kính thủy tinh rất chậm. Thậm chí, khi thử nghiệm trên thép không gỉ, màng mỏng Cu2O/PU cho kết quả xử lý đạt 99,90% virus SARS-CoV-2 trong vòng 1 giờ.
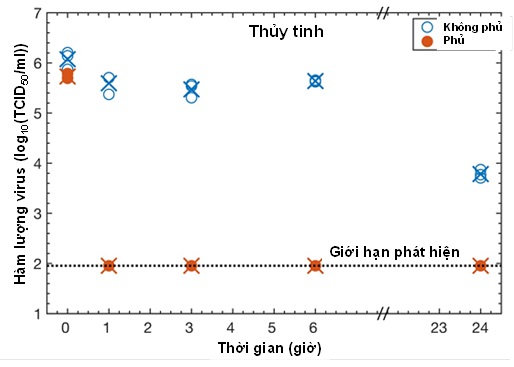
Hình 4. Biến thiên hàm lượng virus SARS-CoV-2 theo thời gian trên bề mặt kính khi không phủ và có phủ Cu2O/PU.
Như vậy, thông qua việc kết hợp Cu2O với PU, nhóm nghiên cứu của GS Ducker đã thành công trong việc tạo ra một hệ màng mỏng Cu2O/PU với chi phí thấp nhưng thể hiện khả năng kháng virus SARS-CoV-2 rất hiệu quả. Đặc biệt, nhờ đặc tính đơn giản, chỉ cần quét lớp polymer PU lên bề mặt rồi bổ sung huyền phù chứa Cu2O, phương pháp tổng hợp này còn cho phép nhóm nghiên cứu dễ dàng ứng dụng lên nhiều bề mặt vật dụng khác nhau, chẳng hạn như tay nắm cửa hay nút bấm trong máy đọc thẻ ATM… (hình 5), qua đó góp phần giúp hạn chế mức độ lây lan của virus này thông qua việc tiếp xúc với bề mặt các vật dụng sử dụng chung.

Hình 5. Ảnh chụp một số vật dụng trước và sau khi phủ màng mỏng Cu2O/PU.
Lê Tiến Khoa (tổng hợp)
TÀI LIỆU THAM KHẢO
[1] N. van Doremalen, N.T. Bushmaker, D.H. Morris, M.G. Holbrook, A. Gamble, B.N. Williamson, A. Tamin, J.L. Harcourt, N.J. Thornburg, S.I. Gerber, J.O. Lloyd-Smith, E. de Wit, V.J. Munster (2020), “Aerosol and surface stability of SARS-CoV-2 as compared with SARS-CoV-1”, N. Engl. J. Med., 382, pp.1564-1567.
[2] A.W.H. Chin, J.T.S. Chu, M.R.A. Perera, K.P.Y. Hui, H.L. Yen, M.C.W. Chan, M. Peiris, L.L.M. Poon (2020), “Stability of SARS-CoV-2 in different environmental conditions”, Lancet Microbe, 1, p.e10.
[3] J. Haldar, D. An, L.A. de Cienfuegos, J. Chen, A.M. Klibanov (2006), “Polymeric coatings that inactivate both influenza virus and pathogenic bacteria”, Proc. Natl. Acad. Sci. U.S.A., 103, pp.17667-17671.
[4] S.Y. Wong, Q. Li, J. Veselinovic, B.S. Kim, A.M. Klibanov, P.T. Hammond (2010), “Bactericidal and virucidal ultrathin films assembled layer by layer from polycationic N-alkylated polyethylenimines and polyanions”, Biomaterials, 31, pp.4079-4087.
[5] EPA Reregistration Eligibility Decision (RED) for Coppers, https://www3.epa.gov/pesticides/chem_search/reg_actions/reregistration/red_G-26_26-May-09.pdf 2009.
[6] D. Chen, D. Zhang, J.C. Yu, K.M. Chan (2011), “Effects of Cu2O nanoparticle and CuCl2 on zebrafish larvae and a liver cell-line”, Aquat. Toxicol., 105, pp.344-354.
[7] I. Amara, W. Miled, R.B. Slama, N. Ladhari (2018), “Antifouling processes and toxicity effects of antifouling paints on marine environment a review”, Environ. Toxicol. Pharmacol., 57, pp.115-130.
[8] G. Borkow (2012), “Safety of using copper oxide in medical devices and consumer products”, Curr. Chem. Biol., 6, pp.86-92.