Vì sao cần đánh giá nguy cơ gãy xương?
Ở cấp độ cá nhân, gãy xương do loãng xương là biến cố lâm sàng nghiêm trọng, do gắn liền với nguy cơ gãy xương tái phát, giảm khả năng vận động, giảm chất lượng cuộc sống và tăng nguy cơ tử vong. Gãy xương có thể xảy ra ở bất kỳ vị trí nào, cũng là dấu hiệu cảnh báo cho gãy xương tiếp theo với nguy cơ tương đối (relative risk-RR) dao động từ 1,4 đến 4,9 tuỳ thuộc vào vị trí gãy (gãy xương hông sẽ tăng nguy cơ gãy xương lần 2 lên 2,8 lần ở nữ và 4,9 lần ở nam) [1]. Hệ quả nghiêm trọng của gãy xương là làm giảm tuổi thọ, nguy cơ tử vong tăng cao ở nam (1,8 lần) hơn ở nữ (1,4 lần). Nghiên cứu của N.D. Syroid, et al. [2] cho thấy, có tới 24% nữ và 38% nam tử vong trong 3 tháng đầu sau khi gãy xương hông; số còn lại thường có tình trạng đau mạn tính, giảm chất lượng cuộc sống và phải phụ thuộc vào sự chăm sóc của người khác.
Ở cấp độ cộng đồng, gãy xương do loãng xương là gánh nặng y tế - xã hội đáng kể, do bệnh rất phổ biến và có chi phí cao. Nguy cơ gãy xương trọn đời được ghi nhận khoảng 50% ở nữ và 30% ở nam. Nguy cơ gãy xương hông cao hơn nguy cơ ung thư vú ở nữ và tương đương với nguy cơ ung thư tiền liệt tuyến ở nam. Các dữ liệu gần đây cho thấy, tần suất gãy xương do loãng xương sẽ tăng nhanh trong vòng vài thập niên tới cùng với tình trạng lão hoá do dân số phát triển nhanh.
Nghiên cứu thử nghiệm lâm sàng (RCT) cho thấy, việc điều trị cho các bệnh nhân có nguy cơ cao bị gãy xương hoặc gãy xương lần đầu sẽ giúp giảm nguy cơ bị gãy xương tái phát từ 30-60%, đồng thời giảm được cả nguy cơ tử vong sau gãy xương (dùng zoledronate trong vòng 3 tháng sau phẫu thuật gãy xương hông giúp giảm 28% nguy cơ tử vong so với người không điều trị) [3]. Tuy nhiên, trong thực tế chỉ có 30% nữ và dưới 10% nam được điều trị loãng xương sau gãy xương.
Nguy cơ gãy xương: không chỉ là mật độ xương thấp?
Nguy cơ gãy xương liên quan tới nhiều yếu tố, nhưng yếu tố quan trọng nhất chính là mật độ xương (MĐX) thấp. Giảm mỗi độ lệch chuẩn của MĐX làm tăng nguy cơ gãy xương lên 2 lần. Vì vậy, mối liên quan giữa MĐX và gãy xương được xem là tương đương, thậm chí mạnh hơn so với mối liên quan giữa cholesterol máu và biến cố tim mạch. Việc đo MĐX được xem là tiêu chuẩn vàng cho chẩn đoán loãng xương ở nữ sau mãn kinh và nam >50 tuổi. Năm 1994, Hội đồng chuyên gia của Tổ chức Y tế thế giới (WHO) đã đề xuất định nghĩa loãng xương ở nữ sau mãn kinh dựa trên MĐX cổ xương đùi giảm ≥2,5 độ lệch chuẩn so với giá trị trung bình của MĐX người trẻ [4]. Tiêu chuẩn này sau đó cũng được áp dụng cho nam và mở rộng cho các vị trí MĐX cột sống và toàn bộ xương hông. Ngoài MĐX thấp, tiền sử gãy xương cá nhân cũng là một yếu tố nguy cơ quan trọng cho gãy xương, với nguy cơ tương đối (RR) dao động từ 1,5 đến 9,5 tuỳ theo độ tuổi gãy, số lần gãy và vị trí gãy.
Các nghiên cứu sâu hơn cho thấy, ngoài MĐX thấp và tiền sử gãy xương, nhiều yếu tố khác như độ tuổi, giới tính, tiền sử gia đình loãng xương, trọng lượng cơ thể thấp, té ngã, hút thuốc lá, sử dụng thuốc glucocorticoid cũng có liên quan mật thiết với nguy cơ gãy xương. Thách thức lớn là làm cách nào để có thể tổng hợp đầy đủ thông tin từ nhiều yếu tố nguy cơ để tiên lượng gãy xương cho một cá nhân. Trong thực hành lâm sàng, người thầy thuốc không thể dựa vào kinh nghiệm và trực giác để đánh giá một lượng lớn thông tin một cách khách quan và chính xác. Các mô hình tiên lượng thống kê với đặc điểm có thể kết hợp khách quan nhiều yếu tố nguy cơ sẽ là cơ sở quan trọng giúp phán đoán lâm sàng chính xác. Một số mô hình tiên lượng gãy xương đã được xây dựng dựa trên phương pháp cá nhân hoá. Hai mô hình phổ biến nhất hiện nay là FRAX và Garvan Fracture Risk. Cả 2 mô hình này đều cung cấp nguy cơ gãy xương trong vòng 5 năm. Ngoài gãy xương nói chung, 2 mô hình còn cung cấp nguy cơ gãy xương hông.
Hiệu quả của các mô hình tiên lượng gãy xương
Hiệu quả của một mô hình tiên lượng sẽ được đánh giá bằng 2 giá trị: độ phân định và độ kiểm định. Phân định là khả năng của mô hình giúp phân biệt cá nhân có nguy cơ cao bị gãy xương khỏi cá nhân không có nguy cơ gãy xương. Giá trị chính của phân định là độ nhạy, độ đặc hiệu thể hiện qua diện tích dưới đường cong ROC (AUC). Trong khi kiểm định đánh giá sự tương thích giữa ca gãy xương quan sát được và xác suất tiên lượng gãy xương ước tính từ mô hình. Trong hơn một thập niên qua, đã có nhiều nghiên cứu độc lập đánh giá hiệu quả của mô hình Garvan, FRAX hoặc cả Garvan và FRAX. Nhìn chung, độ phân định cho gãy xương hông tốt hơn cho gãy xương chung (hình 1).
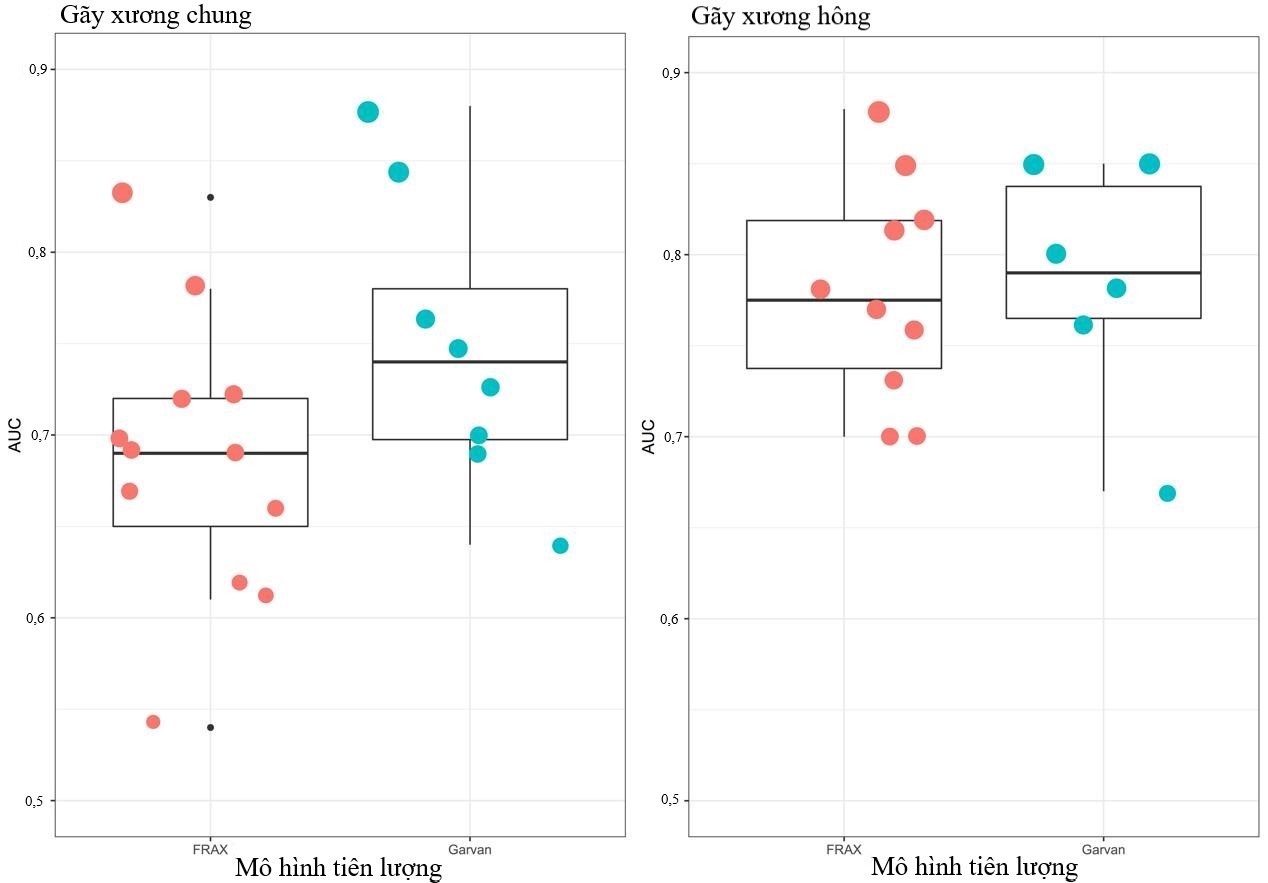
Hình 1. Độ phân định cho gãy xương chung (trái) và gãy xương hông (phải) của mô hình FRAX (đỏ) và Garvan (xanh).
Cho tiên lượng gãy xương chung, giá trị trung bình AUC của Garvan và FRAX lần lượt là 0,76 và 0,69. Cần chú ý giá trị AUC cho những biến cố có tần suất thấp như gãy xương hông thường có tình trạng đánh giá cao hơn thực tế. Độ phân định gãy xương được ghi nhận ở nam thấp hơn ở nữ. Trong nghiên cứu của L. Langsetmo, et al. [5], mô hình Garvan có độ phân định tốt cho gãy xương hông, đặc biệt ở nam (AUC 0,8 cho nữ và 0,85 cho nam). Kết quả từ một nghiên cứu phân tích tổng hợp của A. Marques, et al. [6] cho thấy, AUC trung bình cho gãy xương chung của FRAX là 0,67 (95%CI: 0,64-0,71) và Garvan 0,70 (95%CI: 0,64-0,75).
Trong khi độ phân định giữa FRAX và Garvan là tương đương nhau, thì độ kiểm định của hai mô hình lại rất khác biệt. Hầu hết các nghiên cứu ghi nhận FRAX có xu hướng đánh giá thấp nguy cơ gãy xương (đặc biệt ở bệnh nhân tiểu đường). Một số nghiên cứu cho thấy, Garvan có độ kiểm định tốt, như nghiên cứu trên 1422 phụ nữ sau mãn kinh ở New Zealand ghi nhận độ tương thích của nguy cơ tiên lượng Garvan với các ca gãy xương thực tế lên đến 99%. Nghiên cứu [5] cũng cho thấy độ tương thích cao giữa nguy cơ tiên lượng của mô hình Garvan và các ca gãy xương quan sát trong 10 năm theo dõi. Tuy nhiên, mô hình Garvan có xu hướng ước tính quá mức nguy cơ gãy xương ở nhóm có nguy cơ cao (hình 2).
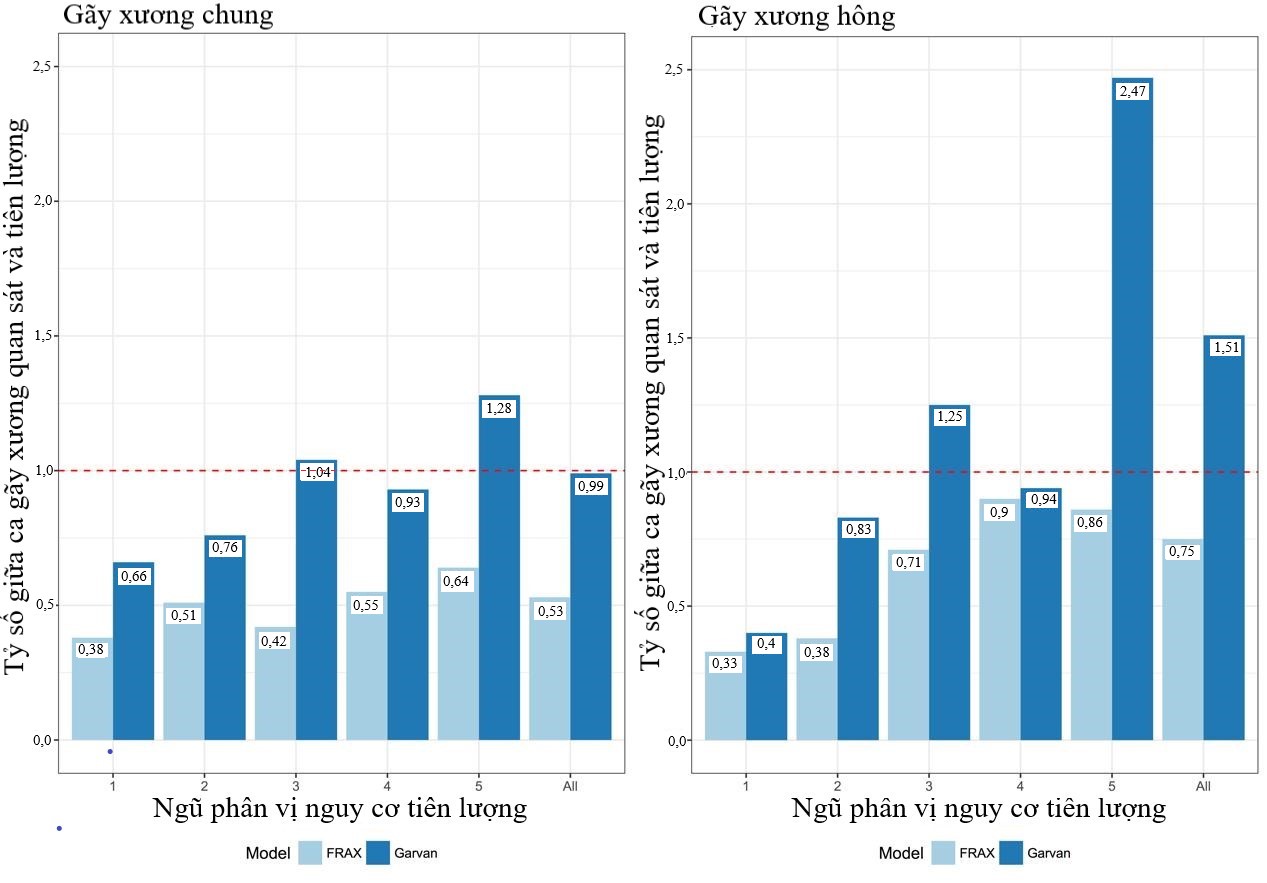
Hình 2. Kiểm định của mô hình FRAX và Garvan.
Kết quả nghiên cứu của T.A. van Geel, et al. [7] đã chỉ ra sự đồng bộ trong xác suất tiên lượng gãy xương giữa Garvan và FRAX rất thấp, với hệ số tương quan là 0,67. Một nguyên nhân giúp giải thích cho sự không đồng bộ này là mô hình Garvan dùng yếu tố nguy cơ tần suất té ngã trong khi FRAX không có. Nghiên cứu kiểm định trên phụ nữ mãn kinh ở Ba Lan cho thấy có sự khác biệt đáng kể giữa 2 mô hình trong ước tính nguy cơ gãy xương, với Garvan có kết quả dự đoán gãy xương chính xác hơn FRAX. Tuy nhiên, phần lớn sự khác biệt giữa FRAX và Garvan không ảnh hưởng đến khuyến cáo điều trị.
Sự không đồng bộ giữa mô hình Garvan và FRAX là không tránh khỏi, do 2 mô hình sử dụng các yếu tố nguy cơ khác nhau. Về bản chất, ước tính nguy cơ là xác suất có điều kiện, phụ thuộc vào các yếu tố được sử dụng và trọng số của các yếu tố này. Ước tính trọng số của mỗi yếu tố phụ thuộc vào phương pháp thống kê được sử dụng để mô hình hoá mối tương quan giữa yếu tố nguy cơ và gãy xương. Trọng số của 5 yếu tố nguy cơ trong mô hình Garvan được thiết lập từ phân tích mô hình Cox đa biến (multivariable Cox's proportional hazards analysis), trong khi phương pháp được sử dụng cho mô hình FRAX là không biến (bảng 1). Do đó, nguy cơ tiên lượng gãy xương của một cá nhân có thể khác nhau tuỳ thuộc vào yếu tố nào được xem xét và không nhất thiết mỗi cá nhân chỉ có một giá trị tiên lượng gãy xương.
|
Đặc điểm
|
Garvan
|
FRAX
|
|
Yếu tố nguy cơ
|
5
|
12
|
|
Điều chỉnh cho nguy cơ tử vong
|
Không
|
Có
|
|
Mô hình thống kê
|
Cox's proportional hazards
|
NA
|
|
Kết quả
|
- Nguy cơ 5 năm và 10 năm của gãy xương chung
- Nguy cơ 5 năm và 10 năm của gãy xương hông
|
- Nguy cơ 10 năm của gãy xương chung
- Nguy cơ 10 năm của gãy xương hông
|
|
AUC cho gãy xương chung
|
0,74 (0,64-0,88)*
|
0,69 (0,54-0,83) *
|
|
AUC cho gãy xương hông
|
0,79 (0,67-0,85) *
|
0,78 (0,70-0,88) *
|
Bảng 1. So sánh mô hình tiên lượng gãy xương FRAX và Garvan.
*Số trung bình và biên độ dao động (trong ngoặc).
Nguồn: T.V. Nguyen, 2017 [8].
Nguy cơ gãy xương ước tính có đồng bộ với hướng dẫn lâm sàng không? Kiểm định 801 nam từ nghiên cứu đoàn hệ theo dõi 10 năm, W. Pluskiewicz, et al. [9] tìm thấy nguy cơ tiên lượng gãy xương của Garvan phù hợp với điều trị tốt hơn FRAX; trong số 218 nam bị gãy xương (có chỉ định điều trị), 82% có nguy cơ Garvan ≥20% so với chỉ có 8% có nguy cơ FRAX ≥20%. Tương tự, ở nhóm có loãng xương (có chỉ định điều trị), tỷ lệ người có nguy cơ ước tính ≥20% là 72% cho Garvan và 10% cho FRAX. Điều này cho thấy, ngưỡng 20% của các mô hình tiên lượng gãy xương phù hợp với các hướng dẫn lâm sàng cho chỉ định điều trị loãng xương.
Tuy nhiên, vẫn chưa biết nếu điều trị các cá nhân có nguy cơ cao được xác định bởi các mô hình tiên lượng, có giúp giảm gãy xương sau đó hay không. Hầu hết các thử nghiệm lâm sàng ngẫu nhiên RCT đánh giá hiệu quả chống gãy xương đều dựa trên tiêu chuẩn MĐX thấp Tscore ≤-2,5 và/hoặc có gãy xương để quyết định chỉ định điều trị. Phần lớn thuốc được ghi nhận có hiệu quả tốt. Cho tới nay, vẫn chưa có nghiên cứu RCT nào được thiết kế đánh giá hiệu quả chống gãy xương dựa trên nguy cơ ước tính từ FRAX hoặc Garvan, do đó chưa xác định được hiệu quả thuốc cho nhóm có yếu tố nguy cơ cao này. Kết quả ban đầu từ phân tích sâu một yếu tố cho thấy, cá nhân có nguy cơ gãy xương cao dựa trên FRAX, giảm được nguy cơ gãy xương khi sử dụng thuốc Denosumab hoặc Baxedoxifene, nhưng không giảm với Strontium Ranelate hoặc Raloxifene. Trong phân tích sâu một yếu tố khác, nhóm nằm trong 25% xác suất gãy xương ước tính cao nhất (trung bình là 24%), điều trị bằng Clodronate giúp giảm 23% nguy cơ gãy xương trong 3 năm và nhóm nằm trong 10% xác suất gãy xương cao nhất (trung bình là 30%), điều trị giúp giảm 31% nguy cơ gãy xương. Các kết quả sơ khởi trên phù hợp với giả thuyết điều trị cho cá nhân có nguy cơ gãy xương cao hoặc trung bình được xác định bằng các mô hình tiên lượng, có thể giảm được gãy xương.
Tại Mỹ, nghiên cứu của A.N. Tosteson, et al. [10] dựa vào hiệu quả kinh tế của mô hình FRAX, ngưỡng chỉ định điều trị được xem xét khi nguy cơ gãy xương hông trong 10 năm là 2,5-4,7% cho nữ, và 2,4-4,9% cho nam. Phụ thuộc vào chi phí y tế của mỗi quốc gia, theo F. Borgstrom, et al. [11], ngưỡng can thiệp của mô hình sẽ thay đổi, tại một số nước khác ngưỡng can thiệp này có thể là 4,0-9,1%. Đối với mô hình Garvan, tại Úc, ngưỡng chỉ định điều trị được xem xét khi nguy cơ gãy xương hông trong 5 năm là 2-5%, trong 10 năm 3-9%; hoặc khi nguy cơ gãy xương chung trong 5 năm là 8-13%, trong 10 năm 14-26%.
Kết luận
Gãy xương do loãng xương là một vấn đề sức khoẻ cộng đồng quan trọng và là biến cố cá nhân nghiêm trọng, do gắn liền với nguy cơ tử vong. Điều trị loãng xương hoặc gãy xương giúp giảm nguy cơ gãy xương tiếp theo. Quan trọng hơn, các chứng cứ mới cho thấy điều trị gãy xương giúp giảm nguy cơ tử vong. Tuy nhiên, tỷ lệ điều trị ở những cá nhân có nguy cơ cao gãy xương vẫn còn rất thấp. Trong 10 năm qua, một số mô hình tiên lượng gãy xương đã được phát triển và sử dụng trong thực hành lâm sàng. Sự tiến bộ của các mô hình này thể hiện thành tựu quan trọng trong lĩnh vực nghiên cứu loãng xương. Thông qua quá trình phát triển, kiểm định và ứng dụng các mô hình này, chúng tôi rút ra một số bài học nổi bật như sau:
Một là, các mô hình tiên lượng gãy xương hiện nay (FRAX, Garvan) có độ phân định khá tốt (AUC từ 0,6 đến 0,8). Độ chính xác của các mô hình rất khác nhau giữa các quần thể. Các chứng cứ cho thấy việc kết hợp thêm các yếu tố mới như profile di truyền, tim bẩm sinh, markers chu chuyển xương vào mô hình hiện nay có thể cải thiện độ chính xác của tiên lượng.
Hai là, đa số các mô hình tiên lượng gãy xương có độ kiểm định kém trong ngoại kiểm. Mô hình FRAX đánh giá thấp, trong khi mô hình Garvan lại đánh giá cao nguy cơ gãy xương. Chưa có sự đồng thuận cho ngưỡng nguy cơ dựa trên mức điều trị hoặc can thiệp.
Ba là, các mô hình tiên lượng tốt nguy cơ gãy xương hông hơn so với gãy xương chung. Điều này cho thấy các mô hình tiên lượng trong tương lai nên được kiểm định riêng biệt cho từng loại gãy xương hơn là “một kích cỡ vừa cho tất cả”.
Bốn là, hiệu quả của các mô hình tiên lượng cá nhân trong thực tế vẫn chưa rõ ràng. Vẫn chưa có câu trả lời chính xác cho vấn đề liệu cung cấp nguy cơ gãy xương tuyệt đối có giúp cải thiện được tỷ lệ chấp nhận điều trị; liệu các cá nhân được xác định là có nguy cơ cao bởi các mô hình khi nhận điều trị có giảm được nguy cơ gãy xương và nguy cơ tử vong sau gãy xương.
Năm là, hiệu quả của các mô hình tiên lượng gãy xương hiện nay trên người châu Á chưa rõ ràng. Chứng cứ từ các nghiên cứu ở người Trung Quốc, Nhật Bản và Hàn Quốc cho thấy, các mô hình này có độ phân định và kiểm định kém.
Sáu là, những tiến bộ trong mô hình thống kê và học máy đã mở ra những cơ hội mới để cải thiện tiên lượng gãy xương. Các mô hình trong tương lai cần giải quyết được sự tương tác và tính chất biến đổi theo thời gian của các yếu tố nguy cơ. Các phương pháp học máy ANN và deep learning là những lựa chọn mới giúp cải thiện độ chính xác của các mô hình tiên lượng.
Mục tiêu cuối cùng của mô hình tiên lượng là cung cấp cho thầy thuốc và bệnh nhân một ước tính nguy cơ chính xác và tái lập, giúp định hướng các quyết định lâm sàng. Các mô hình tiên lượng gãy xương hiện tại đã đóng góp đáng kể vào việc quản lý bệnh nhân loãng xương trong thập niên qua. Tuy nhiên, vẫn cần đẩy mạnh phân định và kiểm định các mô hình này cũng như phát triển các mô hình mới cho người dân châu Á bằng cách sử dụng công nghệ thống kê và học máy giúp tối đa hoá lợi ích ứng dụng trong thực hành lâm sàng.
Cần lưu ý rằng 2 mô hình tiên lượng FRAX và Garvan được phát triển phần lớn dựa vào dữ liệu của người Âu Mỹ và một số dựa vào người Hồng Kông (Trung Quốc) và Nhật Bản. Cả hai nguồn số liệu từ Nhật Bản và Hồng Kông không có chất lượng cao và cũng không phù hợp với người Việt. Trong thực tế, nguy cơ gãy xương ở người Việt có lẽ thấp hơn người Âu Mỹ và yếu tố nguy cơ cũng khác với người Âu Mỹ, nên các ước tính nguy cơ từ các mô hình này chỉ mang tính tham khảo, chứ không thể dựa vào đó để quyết định điều trị.
TÀI LIỆU THAM KHẢO
[1] J.R. Center, D. Bliuc, T.V. Nguyen, J.A. Eisman (2007), "Risk of subsequent fracture after low-trauma fracture in men and women", JAMA, 297(4), pp.387-394.
[2] N.D. Syroid, K.B. Johnson, N.L. Pace, et al. (2010), "Response surface model predictions of emergence and response to pain in the recovery room: An evaluation of patients emerging from an isoflurane and fentanyl anesthetic", Anesth Analg., 111(2), pp.380-386.
[3] P.D. Delmas, R. Rizzoli, C. Cooper, J.Y. Reginster (2005), "Treatment of patients with postmenopausal osteoporosis is worthwhile. The position of the International Osteoporosis Foundation", Osteoporos Int., 16(1), pp.1-5.
[4] J.A. Kanis, L.J. Melton, C. Christiansen, C.C. Johnston, N. Khaltaev (1994), "The diagnosis of osteoporosis", J. Bone. Miner. Res., 9(8), pp.1137-1141.
[5] L. Langsetmo, T.V. Nguyen, N.D. Nguyen, et al. (2011), "Independent external validation of nomograms for predicting risk of low-trauma fracture and hip fracture", CMAJ., 183(2), pp.107-114.
[6] A. Marques, R.J. Ferreira, E. Santos, E. Loza, L. Carmona, J.A. da Silva (2015), "The accuracy of osteoporotic fracture risk prediction tools: a systematic review and meta-analysis", Ann Rheum Dis., 74(11), pp.1958-1967.
[7] T.A. van Geel, N.D. Nguyen, P.P. Geusens, et al. (2011), "Development of a simple prognostic nomogram for individualising 5-year and 10-year absolute risks of fracture: a population-based prospective study among postmenopausal women", Ann Rheum Dis., 70(1), pp.92-97.
[8] T.V. Nguyen, J.A. Eisman (2017), "Fracture risk assessment: from population to individual", J. Clin. Densitom, 20(3), pp.368-378.
[9] W. Pluskiewicz, P. Adamczyk, E. Franek, et al. (2014), "FRAX calculator and Garvan nomogram in male osteoporotic population", Aging Male, 17(3), pp.174-182.
[10] A.N. Tosteson, L.J. Melton, B. Dawson-Hughes, et al. (2008), "Cost-effective osteoporosis treatment thresholds: the United States perspective", Osteoporos Int., 19(4), pp.437-447.
[11] F. Borgstrom, O. Johnell, J.A. Kanis, B. Jonsson, C. Rehnberg (2006), "At what hip fracture risk is it cost-effective to treat? International intervention thresholds for the treatment of osteoporosis", Osteoporos Int., 17(10), pp.1459-1471.