Protein gai của SARS-CoV-2 là gì?
Để hiểu rõ hơn về SARS-CoV-2, chúng ta cùng tìm hiểu cấu trúc của nó. SARS-CoV-2 có khoảng 20 phân tử protein là những thành phần tạo nên cấu trúc của nó (hình 1).
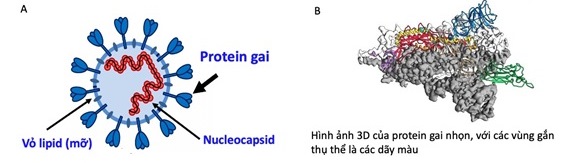
Hình 1. Cấu trúc của SARS-CoV-2 (A) và hình ảnh 3 chiều của protein gai (B).
Hình 1 cho thấy, lõi của SARS-CoV-2 có một đoạn RNA kết hợp với capsid protein gọi là nucleocapsid. Nó được bao bọc bằng một màng lipid (mỡ) bên ngoài - đây chính là lý do mà rửa tay bằng xà phòng là cách diệt virus tốt nhất vì sẽ hòa tan lớp mỡ của nó, khiến virus chết. Trên lớp mỡ này có một số protein gắn vào, mặc dù SARS-CoV-2 sử dụng nhiều loại protein khác nhau để sinh sôi và thâm nhập tế bào, nhưng protein gai là protein bề mặt quan trọng nhất mà virus sử dụng để gắn vào thụ thể trên bề mặt tế bào vật chủ và thâm nhập (hình 1A). Protein gai nhọn của SARS-CoV-2 gồm 1.273 aminoacid, có 75% độ tương đồng với protein gai nhọn của SARS-CoV, cấu trúc 3 chiều của protein này được giải quyết gần đây bởi nhóm của McLellan (hình 1B) [1].
Khả năng siêu lây nhiễm của SARS-CoV-2 bởi những protein gai
SARS-CoV-2 sử dụng protein gai để bám vào protein thụ thể Angiotensin-converting enzyme 2 (ACE2) trên bề mặt tế bào. Nhóm của McLellan [1] đã chứng minh được rằng, khả năng bám vào thụ thể ACE2 của protein gai SARS-CoV-2 lớn hơn gấp 10-20 lần so với SARS-CoV. So sánh trình tự vùng kết nối thụ thể trên gai các coronavirus với nhau cho thấy, vùng kết nối thụ thể của SARS-CoV-2 có ái lực cao với ACE2 của người dựa vào 6 aminoacid chủ lực, so với SARS-CoV thì 5 trong số này là khác hẳn (hình 2) [2].
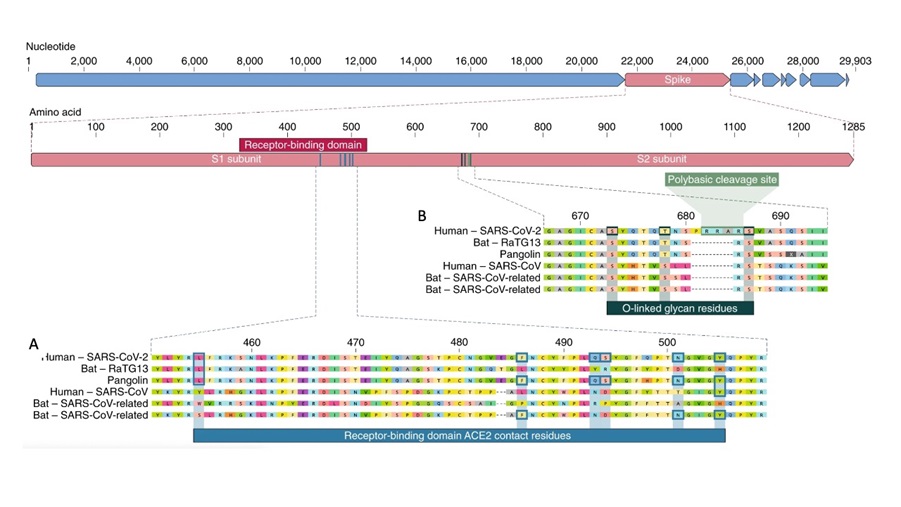
Hình 2. So sánh trình tự protein gai của SARS-CoV-2 và các coronavirus khác.
(A) Trình tự protein của SARS-CoV-2 ngay vùng gắn protein ACE2 (receptor-binding-domain) cho thấy 6 amino acid đặc hiệu của SARS-CoV-2. (B) Vị trí đặc hiệu cắt Furin của SARS-CoV-2 (polybasic cleavage site) chỉ hiện diện trên SARS-CoV-2, không có trên SARS-CoV hay các virus khác.
Ngoài ra, trước khi xâm nhập vào vật chủ, protein gai của SARS-CoV-2 được cắt bằng một số enzymes (men) để quá trình gắn kết vào protein thụ thể trên tế bào vật chủ hiệu quả. Dựa vào phân tích genome trên SARS-CoV-2 so với các coronavirus khác cùng họ như SARS và MERS thì protein gai của SARS-CoV-2 có một vài vị trí đặc hiệu mà enzyme (men) của tế bào người sẽ bám vào và cắt gọt (hình 2). Men đầu tiên có tên là Furin. Chính vị trí kích hoạt nhờ Furin này có lẽ là yếu tố giúp SARS-CoV-2 thâm nhập tế bào dễ dàng, ảnh hưởng đến tính ổn định của virus và khả năng lây lan. Lý do tại sao vị trí gắn Furin trên protein gai của SARS-CoV-2 tăng khả năng thâm nhập của virus vào tế bào người thì chưa rõ. Tuy nhiên, khi chèn trình tự đặc hiệu gắn Furin này vào SARS-CoV và MERS-CoV thì cho thấy chúng lần lượt tăng cường sự hòa nhập vỏ virus SARS-CoV với màng tế bào, cũng như giúp chủng MERS-CoV ở dơi có khả năng xâm nhập tế bào người [2].
Vị trí kích hoạt này cũng được tìm thấy ở protein haemagglutinin (chức năng tương tự protein gai nhọn của SARS-CoV-2) trên những chủng nghiêm trọng của virus cúm mùa [2, 3]. Ngoài ra các nghiên cứu gần đây cho thấy, một số bệnh nhân bị coronavirus cũng có các triệu chứng đường tiêu hoá như tiêu chảy, nôn mửa, đau bụng. Bệnh nhân COVID-19 và SARS có triệu chứng viêm gan (bao gồm suy gan, xác nhận rằng coronavirus có thể nhiễm vào gan). Đường lây lan của SARS-CoV-2 ngoài hô hấp có thể là theo đường phân hoặc miệng [4]. Một điều đáng lưu ý là, tế bào biểu mô thực quản biểu hiện ít thụ thể ACE2 [4, 5]. Có lẽ chính vì sự hiện diện nhiều của Furin trong tế bào ngoài phổi như gan, và ruột non, giải thích tại sao bệnh nhân thường bị tấn công và xuất hiện triệu chứng ở gan và đường tiêu hoá [6-8]. Ngoài ra, nghiên cứu của Zheng và cộng sự vừa đăng trên Nature [9] mô tả rằng, 5/41 bệnh nhân đầu tiên ở Vũ Hán bị tổn thương cơ tim cấp, 4 người phải vào phòng chăm sóc đặc biệt; lý do ngoại trừ việc thụ thể ACE2 hiện diện nhiều trên tế bào cơ tim có lẽ còn là do sự hiện diện rất nhiều của Furin ở tế bào tim (1).
Mục tiêu làm thuốc
Từ những phân tích trên, các nhà khoa học trên thế giới đang tìm kiếm những chất có thể ức chế Furin và ACE2 để làm thuốc. Tất nhiên, đây mới là ý tưởng, việc thực hiện còn mất rất nhiều thời gian. Tuy nhiên, nghiên cứu mới của Walls và cộng sự được đăng trên Cell (một tạp chí chuyên ngành cực kỳ uy tín) cho thấy rằng hướng đi này rất triển vọng [6].
Theo nhóm của Hoffmann [10], một men khác cũng có vai trò rất quan trọng trong cắt gọt protein gai của SARS-CoV-2 là Transmembrane Protease, Serine 2 (TMPRSS2). Nhờ men TMPRSS2 mà protein gai của SARS-CoV-2 được xử lý giúp bám vào thụ thể ACE2 trên người và đi vào tế bào phổi. Ngược lại, việc sử dụng một chất ức chế của TMPRSS2 là Camostat làm giảm rõ rệt khả năng xâm nhập tế bào người của SARS-CoV-2.
Một điều đáng nói khác là Hoffmann, et al. [10] cũng sử dụng huyết thanh của người bệnh SARS hoặc huyết thanh từ thỏ mục tiêu hướng vào protein gai của SARS-CoV và SARS-CoV-2; lấy huyết thanh có kháng thể chống lại protein gai làm giảm khả năng thâm nhập của SARS-CoV-2 vào tế bào chủ (hình 3).
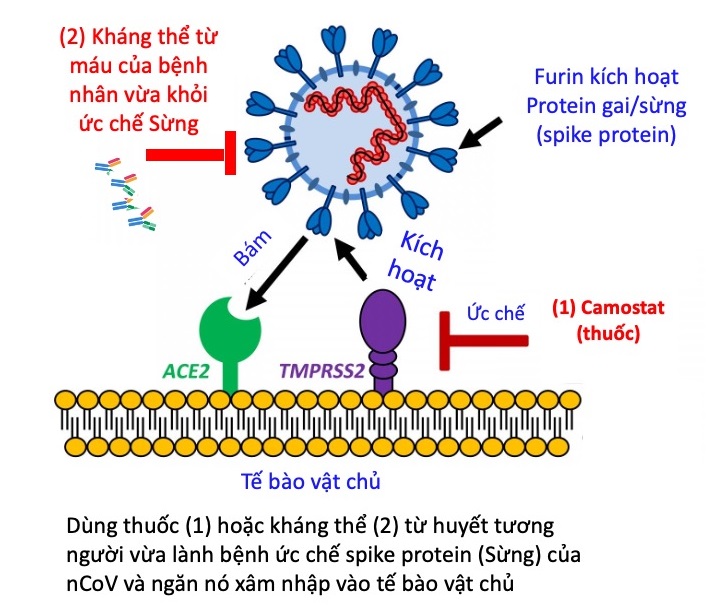
Hình 3. Ý tưởng sử dụng thuốc (1) hoặc kháng thể (2) để ức chế protein gai, ngăn quá trình bám vào thụ thể ACE(2).
Tất cả những kết quả trên cho thấy protein gai của SARS-CoV-2 có vai trò rất quan trọng trong việc thâm nhập, lây lan nhanh chóng của nó. Các khám phá về cấu trúc, trình tự đặc hiệu và cơ chế của protein gai đem lại nhiều triển vọng trong: (1) phát triển vaccine từ cấu trúc 3 chiều của protein nhiều epitope (vị trí gắn đặc hiệu vào kháng thể) sẽ được khám phá; (2) điều trị: ức chế quá trình cắt gọt những protein gai này là một phương pháp tiềm năng làm giảm lượng virus xâm nhập tế bào vật chủ; và (3) ngăn ngừa lây nhiễm từ sự hiểu biết các đường lây lan của SARS-CoV-2.
TÀI LIỆU THAM KHẢO
[1] Wrapp, et al. (2020), “Cryo-EM structure of the SARS-CoV-2 spike in the prefusion conformation”, Science, 367, pp.1260-1263.
[2] Andersen, et al. (2020), “The proximal origin of SARS-CoV-2”, Nature Medicine, https://www.nature.com/articles/s41591-020-0820-9.
[3] Malapaty (2020), “Why does the coronavirus spread so easily between people?” Nature news, Doi: 10.1038/d41586-020-00660-x.
[4] Gu, et al. (2020), “COVID-19: Gastrointestinal manifestations and potential fecal-oral transmission”, Gastroenterology, Doi.org/10.1053/ j.gastro.2020.02.054.
[5] Xiao, et al. (2020), “Evidence for gastrointestinal infection of SARS-CoV-2”, Gastroenterology , Doi.org/10.1053/j.gastro.2020.02.055.
[6] Walls, et al. (2020), “Structure, function and antigenicity of the SARS-CoV-2 spike glycoprotein”, BioRxiv, Doi.org/10.1016/j.cell.2020.02.058.
[7] Jaimes, et al. (2020), “Structural modeling of 2019-novel coronavirus (nCoV) spike protein reveals a proteolytically-sensitive activation loop as a distinguishing feature compared to SARS-CoV and related SARS-like coronaviruses”, BioRxiv, Doi.org/10.1101/2020.02.10.942185.
[8] Coutard, et al. (2020), “The spike glycoprotein of the new coronavirus SARS-CoV-2 contains a furin-like cleavage site absent in CoV of the same clade”, Antiviral Research, Doi: 10.1016/j.antiviral.2020.104742.
[9] Zheng, et al. (2020), “COVID-19 and the cardiovascular system”, Nature, https://www.nature.com/articles/s41569-020-0360-5.
[10] Hoffmann, et al. (2020), “SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and is Blocked by a Clinically Proven Protease Inhibitor”, Cell, 181, pp.1-10.
[11] https://www.drugs.com/international/camostat.html.